 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
已知反应H2+I2=2HI,其速率方程为v=ke(H2)c(I2),该反应()
A.一定是简单反应
B.一定是复杂反应
C.无法确定
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.一定是简单反应
B.一定是复杂反应
C.无法确定
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知反应H2+I2=2HI,其速率方程为v=ke(H2)c(…”相关的问题
更多“已知反应H2+I2=2HI,其速率方程为v=ke(H2)c(…”相关的问题
A.一个单分子反应必为一级反应
B.一个一级反应必为单分子反应
C.H2+I2=2HI的n=2故是双分子反应
D.A+B=C+D是一个二级反应
A.50
B.0.01
C.10
D.无法确定
已知复合反应 是分为以下两步进行的:
是分为以下两步进行的:

则该复合反应的速率方程为().
A、
B、
C、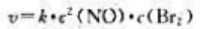
D、
某反应的速率方程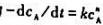 ,其由相同初始浓度开始到转化率达20%所需时间,在40℃时为15min.60℃时为3min.试计算此反应的活化能.
,其由相同初始浓度开始到转化率达20%所需时间,在40℃时为15min.60℃时为3min.试计算此反应的活化能.
有人对反应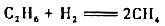 提出如下机理:
提出如下机理:
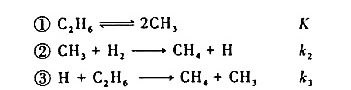
试用稳态近似法和平衡假设法推导生成CH4的速率方程微分表达式,并用已知数据K,k2,k3表示速率常数k。
已知某恒温恒容反应的机理如下:
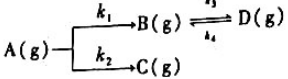
反应开始时只有A(g),且已知CA.o=2.0mol·dm-3,k=3.0s-1,kz=2.5s-1,k3=4.0s-1,k4=5.0s-1.
(1)试写出分别用cA,CB,Cc,CD表示的速率方程;
(2)求反应物A的半衰期;
(3)当反应物A完全反应(即cA=0)时,CB,Cc,CD各为多少?
二氧化氮被臭氧化生成五氧化二氮.其反应机理如下:
①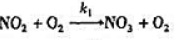 慢
慢
②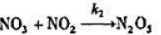 快
快
(1)写出反应方程式及其速率方程;
(2)写出各步反应的活化络合物的结构式及总反应的中间产物的化学式.