 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[单选题]
对于反应,其速率方程为速率常数k的单位为()。
A.s-1
B.mol·L-1·s-1
C.mol-1·L·s-1
D.mol-2·L2·s-1
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.s-1
B.mol·L-1·s-1
C.mol-1·L·s-1
D.mol-2·L2·s-1
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“对于反应,其速率方程为速率常数k的单位为()。”相关的问题
更多“对于反应,其速率方程为速率常数k的单位为()。”相关的问题
有人对反应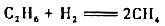 提出如下机理:
提出如下机理:
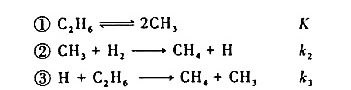
试用稳态近似法和平衡假设法推导生成CH4的速率方程微分表达式,并用已知数据K,k2,k3表示速率常数k。
反应2A→3B的速率方程既可表示为 也可表示为
也可表示为
 则
则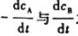 之间的关系为();速率常数kA和kB的关系为().
之间的关系为();速率常数kA和kB的关系为().
实验测得反应
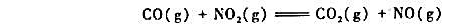
650K时的数据如下:
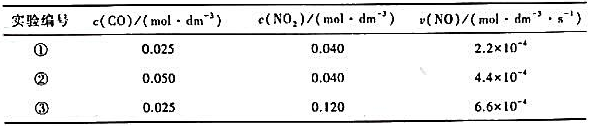
(1)通过推理写出反应的速率方程;
(2)求650K时的速率常数;
(3)当c(CO)=0.10mol·dm-3,c(NO2)=0.16mol·dm-3时,求650K时的反应速率;
(4)若800K时的速率常数为23.0dm3·mol-1·s-1,求反应的活化能。
660K时的反应2NO+02→2NO2NO和O2的初始浓度c(NO)和c(O2)及反应初始速率v的实验数据为:
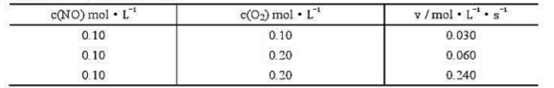
(1)写出反应的速率方程
(2)求反应的级数和速率常数
(3)求c(NO)=c(O2)=0.15molL-1时的反应速率。
250K时化学反应A+2B=2C速率和浓度的关系如下:

(1)写出反应的速率方程,并指出反应指数.
(2)求该反应的速率常数.
(3)求出当c(A)=0.010mol·L-1,c(B)=0.020mol·L-1时的反应速率.
关系为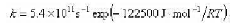 150°C时,由101.325kPa的A开始,到B的分压达到40.023kPa,需多长时间。
150°C时,由101.325kPa的A开始,到B的分压达到40.023kPa,需多长时间。
A.反应速率常数单位为[时间]-1
B.反应物浓度的对数与反应时间呈线型关系
C.半衰期与反应物初始浓度无关
D.消耗75%反应物所需时间为消耗50%反应物所需时间的两倍