 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[单选题]
已知反应N2+3H2=2NH3在等温条件下,标准平衡常数为0.25,那么,在此条件下,反应1/2N2+3/2H2=NH3的标准平衡常数为()。
A.4
B.1
C.2
D.0.5
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.4
B.1
C.2
D.0.5
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知反应N2+3H2=2NH3在等温条件下,标准平衡常数为0…”相关的问题
更多“已知反应N2+3H2=2NH3在等温条件下,标准平衡常数为0…”相关的问题
A.0.1mol・L-1・s-1
B.0.2mol・L-1・s-1
C.0.3mol・L-1・s-1
D.1mol・L-1・s-1
A. 恒温恒压时充入氨气
B. 恒温恒容时充入氮气
C. 恒温恒容时充入氦气
D. 恒温恒压时充入氦气
已知反应N2(g)+3H2(g)=2NH3(g)的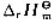 (298.15K)=-92.22kJ·mol-1若升高温度,
(298.15K)=-92.22kJ·mol-1若升高温度,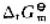 将(),
将(),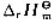 将(),
将(),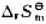 将()、
将()、 将();若减小反应系统体积,平衡将()移动;若加入氨气以增加总压力,平衡将()移动;若加入氢气以增加总压力,平衡将()移动;若加入氯化氧气体、平衡将()移动。
将();若减小反应系统体积,平衡将()移动;若加入氨气以增加总压力,平衡将()移动;若加入氢气以增加总压力,平衡将()移动;若加入氯化氧气体、平衡将()移动。
在等温条件下,对于气体反应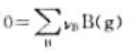 反应的摩尔焓变与摩尔热力学能变之间的关系为()。
反应的摩尔焓变与摩尔热力学能变之间的关系为()。
已知ϕθ(Cu2+/Cu+)=0.153V,ϕθ(I2/I-)=0.536V.
(1)计算ϕθ(Cu2+/CuI)的值.
(2)计算当c(Cu2+)=0.50mol·L-1,c(I-)=0.10mol·L-1时,反应2Cu2++4I-=2Cul+I2的标准平衡常数Kθ.
(3)判断在条件(2)下该反应的自发进行方向.[已知Kspθ(CuI)=1.27X10-12]
A.升高温度使吉布斯自由能变和和标准吉布斯自由能变均增大
B.升高温度可以使平衡向右移动
C.升高温度可以使平衡常数增大
D.正反应自发时,随着反应进行,N2和H2分压逐渐减小,NH3分压逐渐增大,所以平衡常数Kp逐渐增大
反应N2(g)+3H2(g)=2NH3(g)(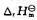 >0)达到平衡后采取下列哪种方法能使平衡向有移动。()
>0)达到平衡后采取下列哪种方法能使平衡向有移动。()
A.加入催化剂
B.降低温度
C.增加H2的压力
D.降低系统的总压