 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
某反应25℃时速率常数为1.3X10-3s-1,35℃时为3.6X10-1s-1.根据范特霍夫规则,估算该反应55℃时的速率常数.
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“某反应25℃时速率常数为1.3X10-3s-1,35℃时为3…”相关的问题
更多“某反应25℃时速率常数为1.3X10-3s-1,35℃时为3…”相关的问题
温度为500K时,某理想气体恒容反应的速率常数 则此反应用压力表示的反应速率常数kp=().
则此反应用压力表示的反应速率常数kp=().
A.11.15
B.31.25
C.21.66
D.0.032
当存在碘催化剂时,氯苯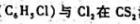 ,溶液中有以下平行二级反应:
,溶液中有以下平行二级反应:
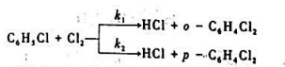
在室温、碘的浓度一定的条件下,当C6H5CI和Cl2在CS2溶液中的初始浓度均为0.5mol.dm-3时,30min后有15%的C6H5CI转化为o-C6H4Cl2有25%的C6H5CI转化为p-C6H4Cl2.试求反应速率常数k1和k2.
实验测得反应
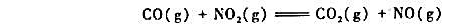
650K时的数据如下:
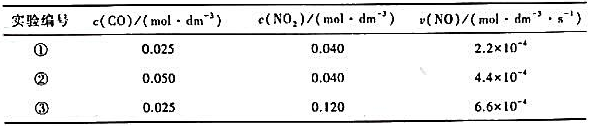
(1)通过推理写出反应的速率方程;
(2)求650K时的速率常数;
(3)当c(CO)=0.10mol·dm-3,c(NO2)=0.16mol·dm-3时,求650K时的反应速率;
(4)若800K时的速率常数为23.0dm3·mol-1·s-1,求反应的活化能。
溶液中某光化学活性卤化物的消旋作用如下:

在正、逆方向上皆为一级反应,且半衰期相等.若原始反应物为纯右旋质,速率常数为 ,试求;
,试求;
(1)右旋物质转化10%所需时间;
(2)24h后的转化率.