 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
对一个电解槽来说,为使电解反应能够进行所必须外加的电压称为()。
A.理论分解电压
B.槽电压
C.实际分解电压
D.电解质溶液压降
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.理论分解电压
B.槽电压
C.实际分解电压
D.电解质溶液压降
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“对一个电解槽来说,为使电解反应能够进行所必须外加的电压称为(…”相关的问题
更多“对一个电解槽来说,为使电解反应能够进行所必须外加的电压称为(…”相关的问题
A.电化学反应中电荷传递不是在同一物理位置上进行,而是在分隔一定距离的两个电极上进行反应
B.电子在电极之间传递是经过参与反应的一个固相(它必须是导体或半导体)
C.电化学反应是在各种化学电池或电解池中实现的
D.电化学反应和一般氧化还原反应都的电子转移发生
某溶液含有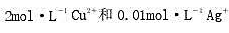 ,若以Pt为电极进行电解。
,若以Pt为电极进行电解。
(1)在阴极上首先析出的是铜还是银?
(2)能否使两种金属离子完全分离?若可以完全分离,阴极电位控制在多少?铜和银在Pt电极上的过电位可忽略不计。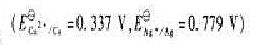
题目来源:1月7日下午山西省大同市面试考题
试讲题目
1.题目:化学平衡
2.内容:
二、化学平衡状态
如果把溶质《不限于固体)在溶液中形成饱和溶被时的状态。称为溶解平衡状态,对于化学反应体系来说,就应当称作化学平衡状态。容解平衡所具有的许多特点,在:化学平衡体系中都可以找到。例如。在反应体系中同时存在着正、道反应两个过程,当这两个过程的速率不相等时,常常只能观购到某个力向的变化。
在一定条件下,当正、逆两个方向的反应速率相等时,反应体系中所有参加反应的物质的质量或浓度可以保持恒定。这时的状态也就是在给定条件下,反应达到了“限度”。对于可逆反应体系来说。我们称之为“化学平衡状态"。这时正、逆变化过程虽然仍在继续,如果不采用特殊的方法或技术,实际观察到的是一种“反应停止了”的表观现象。由此我们可以总结出以下的认识:
1.构成化学平衡体系的基本要求是:反应物和所有产物均处于同一反应体系中,反应条件(如温度、压强等)保持不变。
2.达到化学平衡状态时,体系中所有反应物和生成物的质量(或浓度)保持不变。但是这个体系中的反应并没有停止。只是正、逆反应的速率相等。
我们知道,不同湖度下物质的溶解度不同。那么,t0时达到溶解平衡状态的饱和溶液,当升高或降低温度至t1时,溶解与结晶的速率不再相等。溶解平衡状态被打破,表现为固体溶质继续溶解或析出,直至溶解与结晶的速率再次相等,达到t1下新的溶解平衡状态。
那么化学平衡是否也只有在一定的条件下才能保持?当一个可逆反应达到化学平衡状态后,如果改变浓度,压强。温度等反应条件,平衡状态是否也会发生变化?
有人认为,如果把那些能够进行到底的化学反应体系也看作是可逆性的,亦即相当于正反应的限度接近100%。逆反应的限度几乎等于0的一种情况,就可以把这两类看来似乎迥然不同的反应统一起。不过在定义可逆反应时,有一个必要的前提。那就是,反应物和产物必需同时存在于同一反应体系中,而且在相同条件下,正、逆反应都能够自动进行,不能满足这个前提的化学反应体系,就不能认为是可逆性的。
化学平衡:chemical equilibrium
3.基本要求:
(1)要有适当的情境创设。
(2)教学过程中要有课堂互动环节。
(3)请在十分钟内完成试讲。