 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
下列四组物质反应后生成的气体在水中溶解得到的溶液酸性最强的是()
A.Cu和浓H2SO4
B.CalO3和HCl
C.FeS和HCl
D.CaF2和浓H2SO4
 答案
答案
A、Cu和浓H2SO4
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.Cu和浓H2SO4
B.CalO3和HCl
C.FeS和HCl
D.CaF2和浓H2SO4
 答案
答案
A、Cu和浓H2SO4
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“下列四组物质反应后生成的气体在水中溶解得到的溶液酸性最强的是…”相关的问题
更多“下列四组物质反应后生成的气体在水中溶解得到的溶液酸性最强的是…”相关的问题
)中滴加适量NaOH溶液得白色沉淀(D),加入过量NaOH溶液时,(D)溶解得无色溶液(E)。向(E)中加入NaClO溶液并微热,有棕黑色沉淀(F)生成。将(F)洗净后在一定温度下加热又得(A)。用硝酸处理(A)得沉淀(F)和溶液(C)。向(F)中加入盐酸有白色沉淀(G)和气体(H)生成,(H)可使淀粉碘化钾试纸变蓝。将(G)和KI溶液共热,冷却后有黄色沉淀(Ⅰ)生成。试给出(A),(B),(C),(D),(E),(F),(C),(H)和(I)所代表的物质的化学式,并写出有关化学反应方程式。
,溶于硝酸后经浓缩析出(D)的水合晶体。(D)受热分解得到白色物质(E)和棕色气体(F),将(F)通过NaOH溶液后气体体积变为原来的20%。将(C)通入CuSO4溶液先有浅蓝色沉淀生成,(C)过量后沉淀溶解得深蓝色溶液(G)。试给出(A),(B),(C),(D),(E),(F)和(G)所代表的物质的化学式,并用化学反应方程式表示各过程。
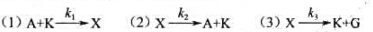 达稳态后,dex/dt=0,求:(1)反应速率-dcA/dt的-般表达式(式中不含X项);(2)k2》k3的反应速率简化表达式:(3)k3>>k2的反应速率简化表达式。
达稳态后,dex/dt=0,求:(1)反应速率-dcA/dt的-般表达式(式中不含X项);(2)k2》k3的反应速率简化表达式:(3)k3>>k2的反应速率简化表达式。
。向(C)的溶液中通入CO2,有白色沉淀(E)析出,(E)不溶于氨水。在较低的温度下加热(E)有(F)生成,(F)易溶于盐酸,也溶于氢氧化钠溶液。但在高温下灼烧(E)后生成的(G)既不溶于盐酸,也不溶于氢氧化钠溶液。试给出(A),(B),(C),(D),(E),(F)和(G)所代表的物质的化学式,并用化学反应方程式表示各过程。
题目来源:1月6日下午江西省南昌市面试考题
试讲题目
1.题目:氦气的性质
2.内容:
氨是没有颜色、有刺激性气味的气体,极易溶解于水且溶解的快。在常温下,1体积的水大约可溶解700体积氨。氦的水溶液叫做氨水。氨溶于水时,大部分与水结合成一水合氨(NH3·H2O)。NH3·H2O很不稳定,受热就会分解为氨和水。
NH3+H2O═NH3·H2O
NH3·H2O═(△)NH3↑+H2O氨水有弱碱性,能使酚酞溶液变红或使红色石蕊试纸变蓝。
资料卡片
氨水为什么显碱性?
在常温下,一水合氨中有一小部分(约1%)电离或NH4+和OH-,所以氨水显弱碱性,能使酚酞溶液变红,按在水中的反应可以表示如下:
NH3+H20═NH3·H2O?NH4++OH-
NH3+H2O═NH4++OH-
氨与酸反应生成铵盐。如氨遇到氯化铵时,迅速反应生成氯化铵晶体。
NH3+HCl═NH4Cl
农业上常用的化肥,如硫酸铵、碳酸氢铵、硝酸铵等都是铵盐。铵盐都易溶于水,受热易分解,与碱反应时放出氨。
NH4Cl═NH3↑+HCI↑
NH4HCO3═(△)NH3↑+CO2↑+H2O
NH4NO3+NaOH═(△)NH3↑+NaNO3+H2O
前面介绍的工业上合成氨的反应是个可逆反应,这说明氨在同一条件下,能自动分解成N2和H2。氨还能被氧气氧化,生成一氧化碳,进而氧化成二氧化碳,用来制造硝酸。
3.基本要求:
(1)要求配合教学内容有简单的板书设计。
(2)教学过程中要有课堂互动环节。
(3)请在十分钟内完成试讲。
答辩题目
1.化学教师需要具备哪些实验教学的能力?
2.喷泉实验成功的关键有哪些?
A.在除氧器内水加热的过程中,水面上蒸汽分压力逐渐增加,气体分压力逐渐降低,使溶解在水中的气体不断地逸出
B.在除氧器内水加热的过程中,水面上蒸汽分压力逐渐增加,气体分压力逐渐增加,使溶解在水中的气体不断地逸出
C.加热除氧的理论基础是气体的溶解定律
D.加热除氧的理论基础是波义尔一马略特定律
色沉淀(C)。(B)溶于硝酸并放出棕色气体(D)。(D)通入NaOH溶液后经蒸发、浓缩析出晶体(E)。(E)受热分解得无色气体(F)和(A)的粉末。试给出(A),(B),(C),(D),(E)和(F)所代表的物质的化学式,并用化学反应方程式表示各过程。