 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
某物质A在有催化剂K存在时发生分解,得产物G。若用X表示A和K所生成的活化络合物,并假设反应按下
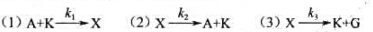 达稳态后,dex/dt=0,求:(1)反应速率-dcA/dt的-般表达式(式中不含X项);(2)k2》k3的反应速率简化表达式:(3)k3>>k2的反应速率简化表达式。
达稳态后,dex/dt=0,求:(1)反应速率-dcA/dt的-般表达式(式中不含X项);(2)k2》k3的反应速率简化表达式:(3)k3>>k2的反应速率简化表达式。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
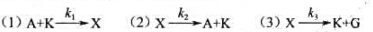 达稳态后,dex/dt=0,求:(1)反应速率-dcA/dt的-般表达式(式中不含X项);(2)k2》k3的反应速率简化表达式:(3)k3>>k2的反应速率简化表达式。
达稳态后,dex/dt=0,求:(1)反应速率-dcA/dt的-般表达式(式中不含X项);(2)k2》k3的反应速率简化表达式:(3)k3>>k2的反应速率简化表达式。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“某物质A在有催化剂K存在时发生分解,得产物G。若用X表示A和…”相关的问题
更多“某物质A在有催化剂K存在时发生分解,得产物G。若用X表示A和…”相关的问题
题目来源:1月6日下午广东省广州市面试考题
试讲题目
1.题目:过氧化氢分解制取氧气
2.内容:
探究:分解过氧化氢制氧气的反应中二氧化锰的作用
注意:仔细观察反应前后的二氧化锰。
1.实验
(1)在试管中加入5mL5%过氧化氢溶液,把带火星的木条伸入试管,观察现象。
(2)向上述试管中加入少量二氧化锰,把带火星的木条伸入试管。观察现象(如图2-15)。
(3)待上述试管中没有现象发生时,重新加入过氧化氢溶液,并把带火星的木条伸入试管,观察现象。待试管中又没有现象发生时,再重复上述操作,观察现象。

图2-15过氧化氢分解实验示意图
2.分析与讨论
(1)在实验(1)和(2)中木条是否复燃?发生这种现象的原因可能是什么?
(2)在实验(3)的重复实验中,反应后二氧化锰有无变化?
(3)综合分析实验(1)~(3)中所观察到的现象,你认为二氧化锰在过氧化氢分解的反应中起了什么作用?
在实验(1)中,带火星的木条不能复燃,是因为过氧化氢溶液在常温下分解缓慢,放出的氧气很少。在实验(2)中,木条复燃,是因为过氧化氢溶液中加入少量二氧化锰,使分解加速。这一反应可以表示如下:

在实验(3)中,实验重复多次,每次只消耗了过氧化氢,二氧化锰好像永远用不完。如果在实验前用精密的天平称量二氧化锰的质量,实验后把二氧化锰洗净、干燥,再称量,你会发现它的质量没有发生变化。把它再加到过氧化氢溶液中,还可以加速过氧化氢分解。这种在化学反应里能改变其他物质的化学反应速率,而本身的质量和化学性质在反应前后都没有发生变化的物质叫做催化剂(又叫触媒)。催化剂在化学反应中所起的作用叫做催化作用。硫酸铜溶液等对过氧化氢的分解也有具有催化作用。
3.基本要求:
(1)教学过程中要有适当的提问环节。
(2)如果需要实验或辅助教学工具,采用语言模拟即可。
(3)要求配合教学内容有适当板书设计。
(4)试讲时间控制在10分钟。
答辩题目
1.如果某一个实验能够用作教师演示实验,有哪些教学要求?
2.如何判断某种物质在化学反应中起到的是催化剂的作用?
A.当簇只包含少量数据点,或者数据点近似协线性时,混合模型也能很好地处理。
B.混合模型比K均值或模糊c均值更一般,因为它可以使用各种类型的分布。
C.混合模型很难发现不同大小和椭球形状的簇。
D.混合模型在有噪声和离群点时不会存在问题
s)=H3(g)+H2S(g).容器内的总压是66.7kPa,一些固体,NH4HS保留在容器中.计算:(1)298.15K时的K值;(2)固体,NH4HS的分解率;(3)如果容器体积减半,容器中周体,NH4HS物质的量如何变化?