 更多“根据标准电极电位数值求算以下反应的平衡常数及.”相关的问题
更多“根据标准电极电位数值求算以下反应的平衡常数及.”相关的问题
第1题
在25℃时测定某一电极反应得下列数据:平均极限扩散电流为3.24mA,求:(1)电极反应的转移电子数;
在25℃时测定某一电极反应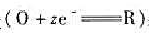 得下列数据:
得下列数据:

平均极限扩散电流为3.24mA,求:
(1)电极反应的转移电子数;
(2)电极反应是否可逆;
(3)假定氧化态和还原态的活度系数和扩散系数相等,计算氧化还原体系的标准电位(相对于SCE)。
第2题
根据表中给出的298K时的热力学数据: 试求算下面反应: 298K时的和该温度下固体表面平衡水汽分
根据表中给出的298K时的热力学数据:

试求算下面反应:

298K时的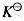 和该温度下固体表面平衡水汽分压。
和该温度下固体表面平衡水汽分压。
第3题
根据标准电极电位数据,判断下列论述是否正确:(1)在Cl-、Br-、I-溶液中,除I卐
根据标准电极电位数据,判断下列论述是否正确:(1)在Cl-、Br-、I-溶液中,除I卐
点击查看答案
根据标准电极电位数据,判断下列论述是否正确:
(1)在Cl-、Br-、I-溶液中,除I-外,其他离子都能被Fe3+氧化。已知: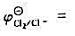

(2)用间接碘量法测定时CuSO4时,Fe3+能氧化I-析出I2,因而干扰CuSO4的测定,加入NH4HF2可消除此干扰。已知: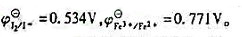
第8题
关于浓差极化,下述哪些说法正确?()
A.浓差极化现象是由于电极过程处于扩散控制过程而产生的;
B.产生浓差极化现象时能斯特方程不能适用;
C.产生浓差极化时,相对于平衡电极电位,阴极电位向正的方向移动;
D.产生浓差极化时,相对于平衡电极电位,阳极电位向正的方向移动

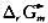 .
.

 如果结果不匹配,请
如果结果不匹配,请 

















