 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在质量为m的单原子组成的晶体中,每个原子可看作在所有其他原子组成的球对称势场V(x)=fr2/2中振动,式中r2=x2+y2+z2.该模型称为三维各向同性谐振子模型,请给出其能级的表达式.
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“在质量为m的单原子组成的晶体中,每个原子可看作在所有其他原子…”相关的问题
更多“在质量为m的单原子组成的晶体中,每个原子可看作在所有其他原子…”相关的问题
某新型超导晶体由镁、镍和碳三种元素组成,镁原子和镍原子一起作面心立方最密堆积,形成有序结构(即无统计原子)。结构中有两种八面体空隙,一种完全由镍原子构成,另一种由镍原子和镁原子共同构成,两种八面体的数量比为1:3,碳原子只填充在由镍原子构成的八面体空隙中。
(1)推断该晶体的结构,并画出该晶体的一个正当晶胞,写出原子在晶胞中的坐标位置;
(2)写出该新型超导晶体的化学式;
(3)指出该晶体的空间点阵型式;
(4)写出两种八面体空隙中心的坐标参数。
本题通过两个箱中粒子模型的应用实例进行运算:
(1)将KCl晶体放置在金属钾蒸气中加热,K原子受辐射而电离,K→K++e-。K+扩散进入晶体,使晶体的K+离子数目多于Cl-离子数目,晶体的组成变为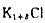 ,为了保持化合物的电中性,电子e-进入负离子的空位代替Cl-,形成
,为了保持化合物的电中性,电子e-进入负离子的空位代替Cl-,形成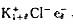 ,晶体显紫红色,这种晶体缺陷结构称色中心。已知Cl-离子半径为181pm,将电子e-看作处于立方体对角线(长为1.73×362pm)作一维势箱运动。试分别求该电子由HOMO→LUMO激发所需的能量以及由LUMO→HOMO所故出光的波长。
,晶体显紫红色,这种晶体缺陷结构称色中心。已知Cl-离子半径为181pm,将电子e-看作处于立方体对角线(长为1.73×362pm)作一维势箱运动。试分别求该电子由HOMO→LUMO激发所需的能量以及由LUMO→HOMO所故出光的波长。
(2)金属钾的摩尔体积室温时为45.36cm3mol-1,试计算它的Fermi能级(EF),分别以J和eV表示,并和实验测定值2.14eV比较。
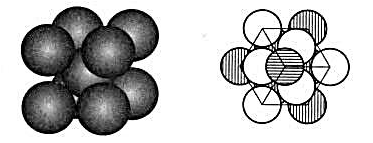
(1)试计算金属晶体中钾原子的空间占有率;
(2)试计算金属晶体中铂原子的空间占有率;
(3)已知铂的相对原子质量为195.08,若金属铂的立方晶胞的边长a=392.3pm,试计算每立方厘米金属铂的质量。
金刚石结构是一种基本的、重要的结构型式,晶体结构所属的空间群为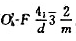 。图C.20.1示出金刚石立方晶胞。
。图C.20.1示出金刚石立方晶胞。
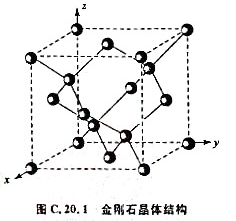
(1)写出两套分别由面心立方点阵联系的C原子坐标参数。
(2)指出平行于z轴、处于(xy)平面的坐标为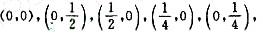
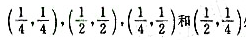 处的四重对移轴的名称相记号。
处的四重对移轴的名称相记号。
(3)通过晶胞中心点有哪些点对称元素,它们组成什么点群?这个点群和Oh点群相同否?
(4)晶体结构属Oh点群,应有对称中心,指出晶跑中对称中心坐标位置。
(5)画出由对称中心联系的两个C原子成键的构象。
(6)指出平行于yz平面的金刚石滑移面d所在位置。
(7)作图示出将图C.20.1去掉一套由面心立方点阵联系的C原子后,余下的晶胞结构图。它属什么点群?有无金刚石滑移面?
(8)作图示出将一套由面心立方点阵联系的C原子换成Si原子,它属什么点群?什么样的结构型式?已知a= 434.8pm,求Si-C键长,讨论这种晶体的性质。
(9)作图示出将图C.20.4中的Si原子换成Ca原子,C原子换成F原子,再在该晶胞中体心和棱心4个位置上加F原子,得成分为CaF2晶体,该晶体属什么点群?结构型式是什么?
(10)作图示出将(9)中所得的CaF2结构的晶胞原点移至Ca原子,分别说明Ca和F原子的配位。
(11)作图示出将图C.20.1中的C换成Si,再在两个Si原子的连线中心点放O原子,指出它的组成,和β-方石英结构比较。
(12)已知β-方石英=730pm,计算它的密度和Si—0键长。
(13)金刚石结构很空旷,如图C.20.1,其中包含许多大空隙,它们的中心位置处在晶胞的棱心和体心。作图示出和C.20.5(a)相似的A2B结构的晶胞(A作原点)中,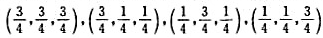 处再加上B原子。分别将相邻的同一种原子画上连接线,指出其结构特点。
处再加上B原子。分别将相邻的同一种原子画上连接线,指出其结构特点。
(14)由(13)题所得结构为NaTl型,已知NaTl立方晶胞参数a=748.8pm,求Tl原子成键情况和Tl-Tl键长。
(15)分析NaTl的结构讨论原子间的结构和该化合物的性质。
A.酚酞由碳、氢、氧元素组成
B.酚酞的相对分子质量为318g
C.酚酞中含有38个原子
D.酚酞中碳元素的质量分数为100%
题目来源:1月7日下午山东省济南市面试考题
试讲题目
1.题目:核外电子的排布规律
2.内容:
原子是由原子核和核外电子构成的。在含有多个电子的原子里,电子分别在能量不同的区域内运动。我们把不同的区域简化为不连续的壳层,也称作电子层(有人把这种电子层模型比拟为洋葱式结构,参看图1),分别用n=1,2,3,4,5,6,7或K,L,M,N,O,P,Q来表示从内到外的电子层。

图1电子层模型示意图
在多电子原子中,电子的能量是不相同的。在离核较近的区域内运动的电子能量较低,在离核较远的区域内运动的电子能量较高。由于原子中的电子是处在原子核的引力场中(类似于地球上的万物处于地心的引力场中),电子总是尽可能地先从内层排起,当一层充满后再填充下一层。那么,每个电子层最多可以排布多少个电子呢?

图2钠原子的核外电子排布
根据原子光谱和理论分析(其中包括元素周期表的启示)的结果,人们得出了原子核外电子排布的规律。
表1核电荷数为1-20的元素原子核外电子层排布

3.基本要求
(1)要求配合教学内容有简单的板书设计。
(2)教学过程中要有课堂互动环节。
(3)请在十分钟内完成试讲。