 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
对于可逆反应H2 (g)+I2 (g)⇌2HI(g),在温度一定下由H2 (g)和I2 (g)开始反应,下列说法正确的是()
A.H2的消耗速率与HI的生成速率之比为2:1
B.若平衡正向移动,则V正一定增大
C.正、逆反应速率的比值是恒定的
D.达到平衡时,正、逆反应速率相等
 答案
答案
D、达到平衡时,正、逆反应速率相等
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.H2的消耗速率与HI的生成速率之比为2:1
B.若平衡正向移动,则V正一定增大
C.正、逆反应速率的比值是恒定的
D.达到平衡时,正、逆反应速率相等
 答案
答案
D、达到平衡时,正、逆反应速率相等
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“对于可逆反应H2 (g)+I2 (g)⇌2HI(g),在温度…”相关的问题
更多“对于可逆反应H2 (g)+I2 (g)⇌2HI(g),在温度…”相关的问题
压力变化不会使下列化学反应的平衡移动的是()。
A.H2(g)+I2(g)→2HI(g)
B.3H2(g)+N2(g)→2NH3(g)
C.2S02(g)+02(g)→2S03(g)
D.C(s)+C02(g)→2CO(g)
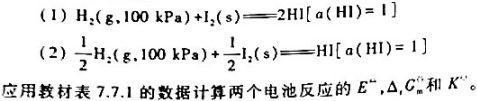
A.50
B.0.01
C.10
D.无法确定
A.增大压力
B.增大D的浓度
C.使用催化剂
D.升高温度
A.达到化学平衡时,4v正(O2) =5v逆(NO)
B.若单位时间内生成n mol NO的同时,消耗n mol NH3,则反应达到平衡状态
C.达到化学平衡时,若增加容器体积,则正反应速率减小,逆反应速率增大
D.化学反应速率关系是:2v正(NH3) =3v正(H2O)
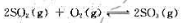
反应达到平衡时,测得混合物中有6.0molSO2(g)。试计算:
(1)该可逆反应在800K时的标准平衡常数和标准摩尔吉布斯自由能变;
(2)SO2在上述条件下的平衡转化率。
由实验测定,反应H2(g)+Cl2(g)=2HCl(g) 的速率方程为: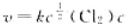 (H2),在其他条件不变的情况下,将每一种反应物的浓度加倍,此时反应速率为()。
(H2),在其他条件不变的情况下,将每一种反应物的浓度加倍,此时反应速率为()。
A.2v
B.4v
C.2.8v
D.2.4v
已知反应:2NO(g)+2H2(g)=N2(g)+2H2O(g)的反应历程为:
①2NO(g)+H2(g)→N2(g)+H2O(g)(慢反应)
②H2O2(g)+H2(g)=2H2O(g)(快反应)
则此反应称为()反应。此两步反应均称为()反应,而反应①称为总反应的(),总反应的速率方程式为(),此反应为()级反应。