 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[多选题]
可逆反应A(g) + 3B(g)==2C(g)+ 2D(s) (正反应为放热反应)达到平衡时,要使正反应速率加快,同时平衡向正反应方向移动,可采取的措施是()
A.增大压力
B.增大D的浓度
C.使用催化剂
D.升高温度
 答案
答案
增大压力
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.增大压力
B.增大D的浓度
C.使用催化剂
D.升高温度
 答案
答案
增大压力
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“可逆反应A(g) + 3B(g)==2C(g)+ 2D(s)…”相关的问题
更多“可逆反应A(g) + 3B(g)==2C(g)+ 2D(s)…”相关的问题
在500 ~ 1000K温度范围内,反应A(g)+B(s)=2C(g)的标准平衡常数Kθ与温度T的关系为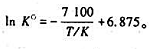 已知原料中只有反应物A(g)和过盘的B(s)。
已知原料中只有反应物A(g)和过盘的B(s)。

半导体工业生产单质硅的过程中有三个重要反应:
(1)二氧化硅被还原为粗硅:SiO2(g)+2C(s)→Si(s)+2CO(g)
(2)硅被氯氧化成四氯化硅:Si(s)+2Cl2(g)→SiCl4(g)
(3)四氯化硅被镁还原生成纯硅:SiCl4(g)+2Mg(s)→2MgCl2(s)+Si(g)
计算上述各反应的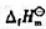 (298K)和生产1.00kg纯硅的总反应热.
(298K)和生产1.00kg纯硅的总反应热.
A.K不变,平衡不移动
B.K不变,平衡右移
C.K变大,平衡不移动
D.K变大,平衡右移
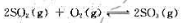
反应达到平衡时,测得混合物中有6.0molSO2(g)。试计算:
(1)该可逆反应在800K时的标准平衡常数和标准摩尔吉布斯自由能变;
(2)SO2在上述条件下的平衡转化率。
已知下列各反应298K时的自由能改变量:
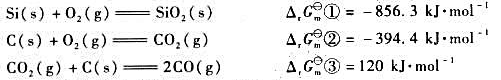
(1)试通过计算说明,制备单质Si的反应:
SiO2(s)+2C(s)=Si(s)+2CO(g)
在常温下不能自发进行。
(2)查热力学数据表,计算上述制备反应的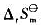 ,进一步计算该反应进行的最低温度要求。
,进一步计算该反应进行的最低温度要求。