 更多“基元反应A(g)+B(g)→D(g)的反应分子数为()。”相关的问题
更多“基元反应A(g)+B(g)→D(g)的反应分子数为()。”相关的问题
A.反应还可细化成多个步骤
B.按反应式表述那样一步完成
C.反应没有经历过渡状态
D.只有反应物分子间才会发生碰撞
在298K及100kPa时,基元反应O3(g)+NO(g)=O2(g)+NO2(g)的活化能为10.7kJ·mol-1,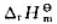 为-193.8kJ·mol-1,其逆反应的活化能为().
为-193.8kJ·mol-1,其逆反应的活化能为().
A.204.5kJ·mol-1
B.183.1kJ·mol-1
C.-183.1kJ·mol-1
D.-204.5kJ·mol-1
(1)写出H2(g),CO(g),CH3OH(I)燃烧反应的热化学方程式;
(2)甲醉的合成反应为:CO(g)+2H2(g)→CH3OH(l).
利用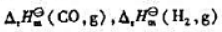
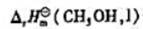 计算该反应的
计算该反应的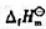 .
.
已知反应:2NO(g)+2H2(g)=N2(g)+2H2O(g)的反应历程为:
①2NO(g)+H2(g)→N2(g)+H2O(g)(慢反应)
②H2O2(g)+H2(g)=2H2O(g)(快反应)
则此反应称为()反应。此两步反应均称为()反应,而反应①称为总反应的(),总反应的速率方程式为(),此反应为()级反应。
1100K时NH3(g)在w上的分解数据如下:

试证明此反应为零级反应,求平均k.
A.Ag2O(s)=2Ag(s)+ O2(g)
O2(g)
B.N2O2=2NO2(g)
C.6C(s)+6H2O(g)=C6H12O6(s)
D.Fe2O3(s)+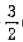 C(s)=2Fe(s)+
C(s)=2Fe(s)+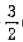 CO2g
CO2g
植物在光合作用中合成葡萄糖的反应可以近似表示为:
6CO2(g)+6H2O(1)=C6H12O6(s)+6O2(g)
计算反应的标准摩尔吉布斯自由能,判断反应在298K及标准状态下能否自发进行,已知葡萄糖的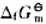 (C6H12O6·s) =-910.5kJ·mol-1。
(C6H12O6·s) =-910.5kJ·mol-1。
化学反应如下:
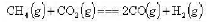
(1)利用附录中各物质的数据,求上述反应在25°C时的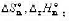
(2)利用附录中各物质的数据,计算上述反应在25°C时的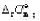
(3)25°C若始态CH4(g)和H2(g)的分压均为150kPa,末态CO(g)和H2(g)的分压均为50kPa,求反应的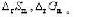


 如果结果不匹配,请
如果结果不匹配,请 

















