 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
反应在某温度时速率系数为2.31×10-3s-1,计算: (1)反应进行了10min后,N2O
反应在某温度时速率系数为2.31×10-3s-1,计算: (1)反应进行了10min后,N2O
反应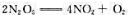 在某温度时速率系数为2.31×10-3s-1,计算:
在某温度时速率系数为2.31×10-3s-1,计算:
(1)反应进行了10min后,N2O5分解的百分率;
(2)N2O,分解反应的半衰期。
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案


 更多“反应在某温度时速率系数为2.31×10-3s-1,计算: (…”相关的问题
更多“反应在某温度时速率系数为2.31×10-3s-1,计算: (…”相关的问题
 则此反应用压力表示的反应速率常数kp=().
则此反应用压力表示的反应速率常数kp=().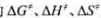 。
。

















