 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
反应C(s)+H2O(g)=CO(g)+H2(g)在一密闭容器中进行。下列说法或结论正确的是()。
A.当v(CO)(正)=v(H2)(正),时,反应达到平衡状态
B.其他条件不变,适当增加C(s)的质量会使平衡正向移动
C.保持容器体积不变,充入少量He使体系压强增大,反应速率一定增大
D.其他条件不变,仅将容器的体积缩小一半,再次达到平衡时,H20(g)的平衡浓度可能是原来的2.1倍
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.当v(CO)(正)=v(H2)(正),时,反应达到平衡状态
B.其他条件不变,适当增加C(s)的质量会使平衡正向移动
C.保持容器体积不变,充入少量He使体系压强增大,反应速率一定增大
D.其他条件不变,仅将容器的体积缩小一半,再次达到平衡时,H20(g)的平衡浓度可能是原来的2.1倍
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“反应C(s)+H2O(g)=CO(g)+H2(g)在一密闭容…”相关的问题
更多“反应C(s)+H2O(g)=CO(g)+H2(g)在一密闭容…”相关的问题
已知反应SnO2(s)+2H2(g)=Sn(s)+2H2O(g)和CO(g)+H2O(g)=CO2(g)+H2(g)的平衡常数分别为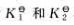 。则反应SnO2(s)+2CO(g)=2CO2(g)+Sn(s)
。则反应SnO2(s)+2CO(g)=2CO2(g)+Sn(s)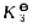 的=()。
的=()。
试用热力学数据表计算823K下以下反应的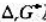 及
及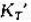 :
:
(1)CoO(s)+H2(g)=Co(s)+H2O(g)
(2)CoO(s)+CO(g)=Co(s)+CO2(g)
并讨论H2和CO还原CoO为Co的可能性,你以为哪种方法更好一些?为什么?
已知反应CO2(g)+H2(g)=CO(g)+H2O(g)在973K时的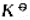 =0.618.若系统中各组分气体分压为p(CO2)=p(H2)=127kPa,p(CO)=p(H2O)=76kPa,计算此时
=0.618.若系统中各组分气体分压为p(CO2)=p(H2)=127kPa,p(CO)=p(H2O)=76kPa,计算此时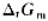 (973K)时值并判断反应进行的方向。
(973K)时值并判断反应进行的方向。
密闭容器中的反应CO(g)+H2O(g)=CO2(g)+H2(g)在750K时其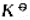 =2.6,试计算:
=2.6,试计算:
(1)当原料气中H2O(g)和CO(g)的物质的量之比为1:1时,CO(g)的转化率为多少?
(2)当原料气中H2O(g)和CO(g)的物质的量之比为4:1时,CO(g)的转化率为多少 ? 说明什么问题?
A.在温度升高至一定数值以上即可自发进行
B.在温度降低至一定数值以上即可自发进行
C.在任何温度下反应都能自发进行
D.在任何温度下反应都不能自发进行
298K时,反应BaCl2·2H2O(s) BaCl2(s)+2H2O(g)达到平衡时,p(H2O)=330Pa,求反应的
BaCl2(s)+2H2O(g)达到平衡时,p(H2O)=330Pa,求反应的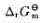 。
。
A.CO(g)+Cl2(g)→COCl2(g)
B.2NO2(g)→NO(g)+1/2O2(g)
C.N2(g)+O2(g)→2NO(g)
D.NH4HS(s)→NH3(g)+H2S(g)
在373K下,反应:COCI2(g)===CO(g)+Cl2(g)的Kp=8×109,ΔSƟ373=125.5J/K。
计算:(1)373K,总压为202.6kPa时COCl2的解离度;
(2)373K下上述反应的ΔHƟ:
(3)总压为200kPa,COCl2的解离度为0.1%时的温度,设ΔCp=0。
题目来源:1月7日上午河南省郑州市面试考题
试讲题目
1.题目:硫酸的制备
2.内容:
如果以硫黄为原料制硫酸,你能试着用化学方程式表示制硫酸的反应原理吗?
目前,工业上制硫酸的基本生产原理如下:
1.以硫为原料制备SO2
S(s)+O2(g)═SO2(g)(放热反应)
2.利用催化氧化反应将SO2氧化成SO3
2SO2(g)+O2(g)═(催化剂)2SO3(g)(放热反应)
3.三氧化硫转化为硫酸
SO3(g)+H2O(l)═H2SO4(l)(放热反应)
按照上述反应原理,工业上制硫酸主要分造气、催化氧化和吸收三个阶段。

图1-2硫酸工业流程
在生产中还应考虑许多实际问题,如原料的净化、反应条件及设备的选择、废热的利用等。