 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
一个手电筒由电池电动势4.5V供电,已知电池内阻为0.5欧姆,如果手电筒灯泡流过电流为1A,则灯泡电阻为()
A.1欧姆
B.2欧姆
C.3欧姆
D.4欧姆
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.1欧姆
B.2欧姆
C.3欧姆
D.4欧姆
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“一个手电筒由电池电动势4.5V供电,已知电池内阻为0.5欧姆…”相关的问题
更多“一个手电筒由电池电动势4.5V供电,已知电池内阻为0.5欧姆…”相关的问题
25℃时测得下列电池的电动势为0.622V,求配合物Ag(CN)2-的稳定常数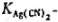 。(已知
。(已知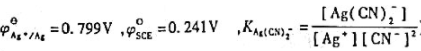 )
)
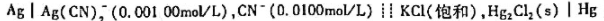
下列电池的电动势为0.460V。计算反应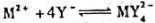 生成的配合物
生成的配合物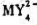 的稳定常数
的稳定常数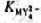 (已知
(已知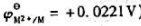 )。
)。
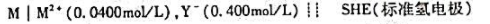
电池:(一)玻璃电极|缓冲溶液(pH=4.03)||饱和甘汞电极(),测得电动势为0.270V,当已知pH的缓冲溶液换成某一未知液时,测得电动势为0.304V,求未知液的pH。
答:
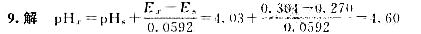
测得下列电池的电动势为0.792V(25℃);
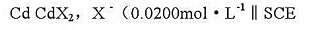
已知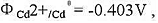 忽略液接电位,计算CdX2的Ksp.(CdX2为镉的难溶盐)
忽略液接电位,计算CdX2的Ksp.(CdX2为镉的难溶盐)
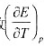
为1.40x10-4V/K。
已知电池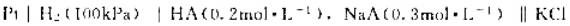 (饱和)|Hg2Cl2|Hg的电动势为0.762V,
(饱和)|Hg2Cl2|Hg的电动势为0.762V,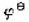 =0.244V,求HA的解离常数(忽略液接电位及离子强度)。
=0.244V,求HA的解离常数(忽略液接电位及离子强度)。
25℃时,实验测得以下三个电池的电动势如下:
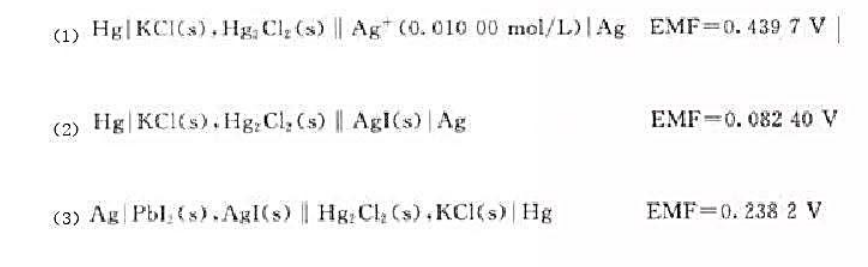
请用实验数据,计算AgI和PbI2的溶度积。已知饱和甘汞电极的电极电位为0.2415V。
已知铅酸蓄电池
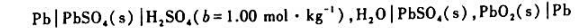
在25°C时的电动势E=1.9283V,Eθ=2.0501V.该电池的电池反应为
Pb(s)+PbO2(s)+2SO42-+4H+→2PbSO4(s)+2H2O
(1)请写出该电池的电极反应;
(2)计算该电池中硫酸溶液的活度a、平均离子活度az及平均离子活度因子γz;
(3) 已知该电池的温度系数为5.664x10-5V·K-1,计算电池反应的ΔrGm,ΔrSm,ΔrHm,
及可逆热Qr,m.
已知298K时下述电池的电动势为1.362V,
(Pt)H2(pθ)|H2SO4(aq)|Au2O3=Au(s)
又知H2O(g)的ΔrGmθ=-228.6kJ·mol-1,该温度下水的饱和蒸汽压为3167Pa,
求在298K时氧气的逸度为多少才能使Au2O3与Au呈平衡?
甲烷燃烧过程可设计成燃料电池.当电解质为酸性溶液时,电极反应和电池反应分别为
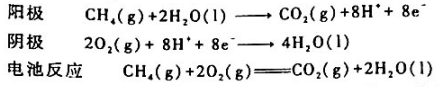
已知,25°C时有关物质的标准摩尔生成吉布斯函数 为
为
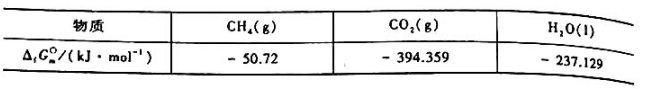
计算25°C时该电池的标准电动势.