 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
25℃时,实验测得以下三个电池的电动势如下:请用实验数据,计算AgI和PbI2的溶度积。已知饱和甘
25℃时,实验测得以下三个电池的电动势如下:
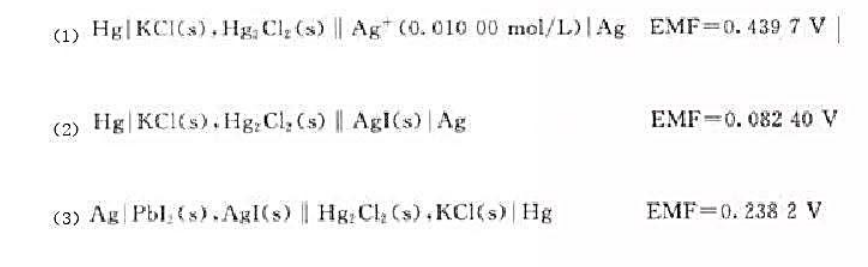
请用实验数据,计算AgI和PbI2的溶度积。已知饱和甘汞电极的电极电位为0.2415V。
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
25℃时,实验测得以下三个电池的电动势如下:
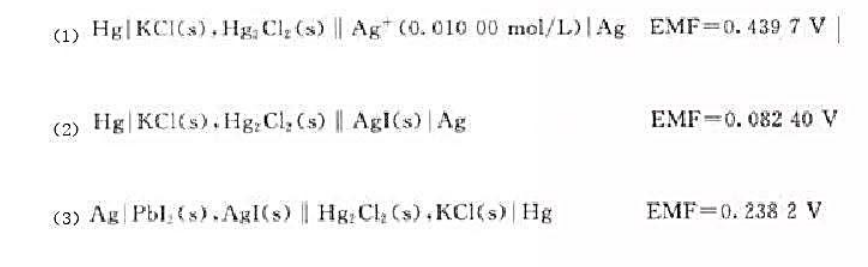
请用实验数据,计算AgI和PbI2的溶度积。已知饱和甘汞电极的电极电位为0.2415V。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“25℃时,实验测得以下三个电池的电动势如下:请用实验数据,计…”相关的问题
更多“25℃时,实验测得以下三个电池的电动势如下:请用实验数据,计…”相关的问题
25℃时测得下列电池的电动势为0.622V,求配合物Ag(CN)2-的稳定常数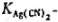 。(已知
。(已知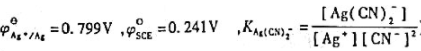 )
)
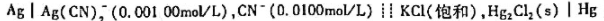
电池: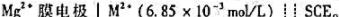 。在25℃时,测得电动势为0.387V。
。在25℃时,测得电动势为0.387V。
(1)当用未知溶液代替上述已知Mg2+溶液时。测得电池电动势为0.425V,求此溶液的pMg为多大?
(2)若溶液替代引起液接电位Ej的不稳定值为±1mV,则Mg2+浓度测定产生的相对误差有多大?波动范围为多少?
以Ag/AgC1与铜离子选择性电极组成下列电池饱和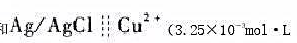
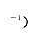 铜离子选择性电极
铜离子选择性电极
在25℃时,测得电池的电动势为0.124V。若用未知铜活度的溶液取代上述电池中Cu2+(3.25X10-3mo1•L-1)的溶液,测得其电动势为0.086V。计算未知液中pCu(不考虑液接电位)。
测得下列电池的电动势为0.792V(25℃);
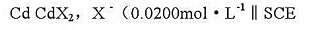
已知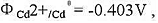 忽略液接电位,计算CdX2的Ksp.(CdX2为镉的难溶盐)
忽略液接电位,计算CdX2的Ksp.(CdX2为镉的难溶盐)
为测定下列吡啶与水之间的质子转移反应的平衡常数,
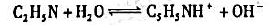
安装以下电池:
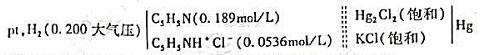
若25℃时电池电动势为0.563V,上述反应的平衡常数Kb为多少?
电池:(一)玻璃电极|缓冲溶液(pH=4.03)||饱和甘汞电极(),测得电动势为0.270V,当已知pH的缓冲溶液换成某一未知液时,测得电动势为0.304V,求未知液的pH。
答:
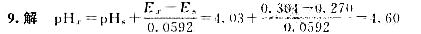
25℃时,下列电池的电动势为0.518V(忽略液接电位):
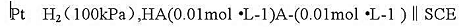
计算弱酸HA的Ka值.