 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[单选题]
对峙基元反应在一定条件下达到平衡时,下列描述不正确的是()。
A.正逆向反应速率相等
B.正逆向反应速率常数相等
C.各物质浓度不再随时间变化
D.温度升高,通常正逆向反应速率都增大
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.正逆向反应速率相等
B.正逆向反应速率常数相等
C.各物质浓度不再随时间变化
D.温度升高,通常正逆向反应速率都增大
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“对峙基元反应在一定条件下达到平衡时,下列描述不正确的是()。”相关的问题
更多“对峙基元反应在一定条件下达到平衡时,下列描述不正确的是()。”相关的问题
已知反应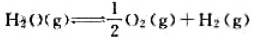 在一定温度、压力下达到平衡。此后通入氛气,若保持反应的压力、温度不变,则有().
在一定温度、压力下达到平衡。此后通入氛气,若保持反应的压力、温度不变,则有().
A.平衡向左移动
B.平衡向右移动
C.平衡保持不变
D.无法预测
在500K时将 在体积为15.0L的容器内达到下列化学平衡:
在体积为15.0L的容器内达到下列化学平衡: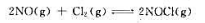 当反应在500K达到化学平衡后测得容器内NaCl的物质的量为3.06mol,计算该温度下NO的平衡物质的量和反应的标准平衡常数。
当反应在500K达到化学平衡后测得容器内NaCl的物质的量为3.06mol,计算该温度下NO的平衡物质的量和反应的标准平衡常数。
五氧化二磷(PCI3)分解反应
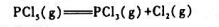
在200℃时的K°=0.312,计算:
(1)200℃,200kPa下PCI3的解离度;
(2)摩尔比为1:5的PCI3与CI2的混合物,在200℃,100kPa下达到平衡时PCI3的解高度.
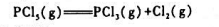
A.一定大于零
B.一定小于零
C.一定等于零
D.既可能大于零,也可能小于零
A.恒温封闭的体系是平衡建立的前提
B.正反应和逆反应的速率相等
C.是一个封闭体系中,可逆反应进行的最大限度达到平衡之后,各物质浓度不再随着时间变化而变化
D.化学平衡只能在一定条件下才能保持
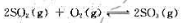
反应达到平衡时,测得混合物中有6.0molSO2(g)。试计算:
(1)该可逆反应在800K时的标准平衡常数和标准摩尔吉布斯自由能变;
(2)SO2在上述条件下的平衡转化率。