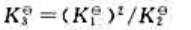题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
下列可逆反应: 在2000K时设在此温度下有由CO、O2和CO2组成的混合气体,它们的分压分
下列可逆反应:
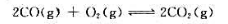
在2000K时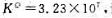 设在此温度下有由CO、O2和CO2组成的混合气体,它们的分压分别为1kPa、5kPa和100kPa,试计算此条件下反应的摩尔吉布斯自由能变。反应向哪个方向进行?如果CO和CO2的分压不变,要使反应向逆反应方向进行,O2的分压应是多少?
设在此温度下有由CO、O2和CO2组成的混合气体,它们的分压分别为1kPa、5kPa和100kPa,试计算此条件下反应的摩尔吉布斯自由能变。反应向哪个方向进行?如果CO和CO2的分压不变,要使反应向逆反应方向进行,O2的分压应是多少?
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
下列可逆反应:
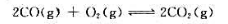
在2000K时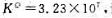 设在此温度下有由CO、O2和CO2组成的混合气体,它们的分压分别为1kPa、5kPa和100kPa,试计算此条件下反应的摩尔吉布斯自由能变。反应向哪个方向进行?如果CO和CO2的分压不变,要使反应向逆反应方向进行,O2的分压应是多少?
设在此温度下有由CO、O2和CO2组成的混合气体,它们的分压分别为1kPa、5kPa和100kPa,试计算此条件下反应的摩尔吉布斯自由能变。反应向哪个方向进行?如果CO和CO2的分压不变,要使反应向逆反应方向进行,O2的分压应是多少?
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“下列可逆反应: 在2000K时设在此温度下有由CO、O2和C…”相关的问题
更多“下列可逆反应: 在2000K时设在此温度下有由CO、O2和C…”相关的问题
已知可逆反应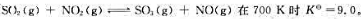 若在此温度下,SO2、NO2、SO2和NO的分压都为50kPa,试通过计算判断反应进行的方向。
若在此温度下,SO2、NO2、SO2和NO的分压都为50kPa,试通过计算判断反应进行的方向。
已知四氧化二氮的分解反应如下:

在298.15K时,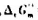 =4.75kJ·mol-1.试判断在此温度及下列条件下,反应进行的方向.
=4.75kJ·mol-1.试判断在此温度及下列条件下,反应进行的方向.
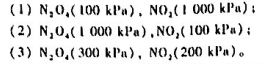
已知可逆反应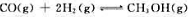 在523K和548K时的标准平衡常数分别为2.3×10-3和5.4×10-4,该可逆反应在一定条件下达到了化学平衡。当升高温度时,化学平衡向()方向移动;加入催化剂后,化学平衡()。
在523K和548K时的标准平衡常数分别为2.3×10-3和5.4×10-4,该可逆反应在一定条件下达到了化学平衡。当升高温度时,化学平衡向()方向移动;加入催化剂后,化学平衡()。
如附图所示是碳的相图,试根据该图回答下列问题:
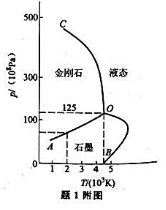
(1)说明曲线OA,OB,OC分别代表什么?
(2)说明点O的含义:
(3)碳在室温及101.325kPa下,以什么状态稳定存在?
(4)在2000K时,增加压力,使石墨转变成金刚石是一个放热反应,试从相图判断两者的摩尔体积Vm哪个大?
(5)从图上估计2000K时,将石墨变为金刚石需要多大压力?
973K时,下列可逆反应的标准平衡常数分别为
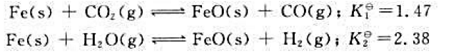
试计算如下可逆反应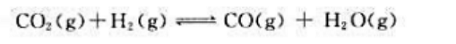 在973K时的标准平衡常数。
在973K时的标准平衡常数。
已知温度T时可逆反应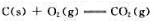 的标准平衡常数为
的标准平衡常数为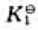 ,可逆反应
,可逆反应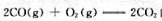 的标准平衡常数为
的标准平衡常数为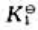 ,则可逆反应
,则可逆反应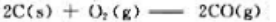 的标准平衡常数
的标准平衡常数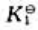 为()。
为()。
A、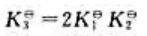
B、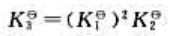
C、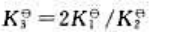
D、