 更多“ 混床失效后,再生前通入NaOH的目的是什么?”相关的问题
更多“ 混床失效后,再生前通入NaOH的目的是什么?”相关的问题
第5题
无色钠盐晶体(A)溶于水后,加入AgNO3溶液有浅黄色沉淀(B)生成。用NaOH溶液处理(B),得到棕黑
无色钠盐晶体(A)溶于水后,加入AgNO3溶液有浅黄色沉淀(B)生成。用NaOH溶液处理(B),得到棕黑
点击查看答案
色沉淀(C)。(B)溶于硝酸并放出棕色气体(D)。(D)通入NaOH溶液后经蒸发、浓缩析出晶体(E)。(E)受热分解得无色气体(F)和(A)的粉末。试给出(A),(B),(C),(D),(E)和(F)所代表的物质的化学式,并用化学反应方程式表示各过程。
第7题
用水处理短周期元素形成的黄色二元化合物(A),得到白色沉淀(B)和无色气体(C)。(B)不溶于NaOH溶液
用水处理短周期元素形成的黄色二元化合物(A),得到白色沉淀(B)和无色气体(C)。(B)不溶于NaOH溶液
点击查看答案
,溶于硝酸后经浓缩析出(D)的水合晶体。(D)受热分解得到白色物质(E)和棕色气体(F),将(F)通过NaOH溶液后气体体积变为原来的20%。将(C)通入CuSO4溶液先有浅蓝色沉淀生成,(C)过量后沉淀溶解得深蓝色溶液(G)。试给出(A),(B),(C),(D),(E),(F)和(G)所代表的物质的化学式,并用化学反应方程式表示各过程。
第10题
题目来源:1月7日上午山东省青岛市面试考题试讲题目1.题目:从铝土矿中提取铝2.内容:氯元素占地壳
题目来源:1月7日上午山东省青岛市面试考题
试讲题目
1.题目:从铝土矿中提取铝
2.内容:
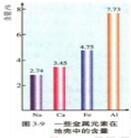
氯元素占地壳总量的7.73%,是地充中含量最多的金属元素。铝土矿(主要成分为Al2O3,还有少量杂质)是氯元素在地壳中的主要存在形式之一。要从铝土矿中提取铝,必须获得纯度较高的氧化铝。从铝土矿中提取铝的工艺流程如图所示。

图从铝土矿中提取铝的工艺流程
由上述生产工艺流程可知,铝土矿与氢氧化钠溶液混合时,铝土矿中的Al2O3与NaOH能发生反应,生成可溶于水的NaA1O2。将反应得到的混合物过滤,除去残
渣,向滤液中通入过量CO2气体,将其酸化,NaA1O2便将转为Al(OH)3沉淀析出。
在高温下灼烧Al(OH)3,生成Al2O3。
2A1(OH)3═(△)Al2O3+3H2O
氧化铝较稳定,很难用还原剂还原。工业上采用电解熔融氧化铝的方法冶炼铝。
2Al2O3═(通电)4Al+3O2↑
3.基本要求:
(1)教学中要有适当板书;
(2)教学中要有提问互动环节;
(3)如果教学过程中有实验操作,用语言进行情境模拟即可。


 如果结果不匹配,请
如果结果不匹配,请 

















