 更多“硅砂的主要成分是()”相关的问题
更多“硅砂的主要成分是()”相关的问题
第5题
半导体工业生产单质硅的过程中有三个重要反应:(1)二氧化硅被还原为粗硅:SiO2(g)+2C(s)→Si
半导体工业生产单质硅的过程中有三个重要反应:(1)二氧化硅被还原为粗硅:SiO2(g)+2C(s)→Si
点击查看答案
半导体工业生产单质硅的过程中有三个重要反应:
(1)二氧化硅被还原为粗硅:SiO2(g)+2C(s)→Si(s)+2CO(g)
(2)硅被氯氧化成四氯化硅:Si(s)+2Cl2(g)→SiCl4(g)
(3)四氯化硅被镁还原生成纯硅:SiCl4(g)+2Mg(s)→2MgCl2(s)+Si(g)
计算上述各反应的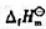 (298K)和生产1.00kg纯硅的总反应热.
(298K)和生产1.00kg纯硅的总反应热.
第10题
试解释下列现象:(1)碳与硅为同族元素,但其氧化物CO2,SiO2性质上相差极大.(2)NaCl与AgC
试解释下列现象:(1)碳与硅为同族元素,但其氧化物CO2,SiO2性质上相差极大.(2)NaCl与AgC
点击查看答案
试解释下列现象:
(1)碳与硅为同族元素,但其氧化物CO2,SiO2性质上相差极大.
(2)NaCl与AgCl化合物中阳离子都为+1,但AgCl难溶于水,NaCl易溶于水.
(3)第三周期元素氟化物熔点从SiF4开始突然下降:NaF(980℃),MgF2(1400℃),AlF3(1040℃),SiF4(-77℃),PF5(-83℃),SF6(-55℃).
(4)BeO熔点高于LiF,而FeCl3熔点又低于FeCl2.
(5)HgS,CdS,ZnS颜色差异.
第11题
()是由硅砂、石灰石、萤石等矿物在熔炉中熔化后以喷制或拉制而成,产品具有密度小、孔隙大、热导率低、吸声系数高、吸水率低等特点。
A.岩棉制品
B.玻璃棉制品
C.酚醛泡沫
D.膨胀珍珠岩


 如果结果不匹配,请
如果结果不匹配,请 

















