 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
容器中放有CO2和N2,温度为25℃,其分压均为1bar,则pCO2=(),pN2=()。
容器中放有CO2和N2,温度为25℃,其分压均为1bar,则pCO2=(),pN2=()。
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“容器中放有CO2和N2,温度为25℃,其分压均为1bar,则…”相关的问题
更多“容器中放有CO2和N2,温度为25℃,其分压均为1bar,则…”相关的问题
容器中放有CO2和N2,温度为25℃,其分压均为1bar,则xco2=() ,xN2=() 。
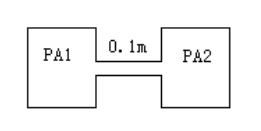
g)和H2O(l)。过程放热401.727kJ。求
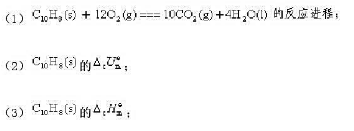
密闭容器中的反应CO(g)+H2O(g)=CO2(g)+H2(g)在750K时其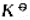 =2.6,试计算:
=2.6,试计算:
(1)当原料气中H2O(g)和CO(g)的物质的量之比为1:1时,CO(g)的转化率为多少?
(2)当原料气中H2O(g)和CO(g)的物质的量之比为4:1时,CO(g)的转化率为多少 ? 说明什么问题?
25℃,200kPa下,将4mol的纯A(g)放入带活塞的密闭容器中,达到如下化学平衡:
A(g)=2B(g).已知平衡时nA=1.697mol,nB=4.606mol.
(1)求该温度下反应的Kθ和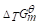 ;
;
(2)若总压为50kPa,求平衡时A,B的物质的量.