题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
下面是氧元素的电势图: 试据此计算H2O的离子积常数kw。
下面是氧元素的电势图:
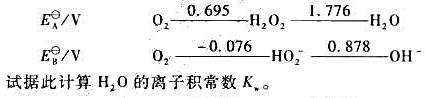
试据此计算H2O的离子积常数kw。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
下面是氧元素的电势图:
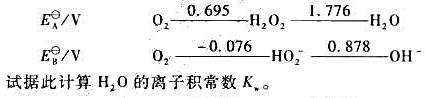
试据此计算H2O的离子积常数kw。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“下面是氧元素的电势图: 试据此计算H2O的离子积常数kw。”相关的问题
更多“下面是氧元素的电势图: 试据此计算H2O的离子积常数kw。”相关的问题
根据下面pH=1的酸性介质中Bi的元素电势图:

(2)作出Bi元素的自由能一氧化数图。
将电对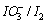 和
和 电对的电势-pH图画在同一直角坐标系中。指出体系中涉及的歧化反应和逆歧化反应发生的具体pH范围。若在298K,pH=11时将所发生的反应以原电池方式完成,试计算原电池的电动势E和电池反应的
电对的电势-pH图画在同一直角坐标系中。指出体系中涉及的歧化反应和逆歧化反应发生的具体pH范围。若在298K,pH=11时将所发生的反应以原电池方式完成,试计算原电池的电动势E和电池反应的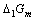 。
。
题目来源:1月7日上午江苏省泰州市面试考题
试讲题目
1.题目:氢键的形成
2.内容:
氧和硫同为VIA族元素,H2O和H2S的结构也很相似。从相对分子质里对分子间作用力和物质性质影响的角度分析,应该是H2S的沸点高于H2O,但通常情况下,H2O是液体(沸点为100℃),H2S是气体(沸点为-61℃)。你知道导致H2O沸点反常的原因吗?

图一些氧化物的沸点
水分子中的O-H键是极性共价键,氧原子与氢原子共用的电子对强烈地偏向氧原子,使H原子几乎成了“裸露”的质子。这样,一个水分子中相对显正电性的氢原子,就能与另一个水分子中相对显负电性的氧原子的孤对电子对接近并产生相互作用,这种相互作用叫做氢键(hydrogen bond)
氢键是一种既可以存在于分子之间又可以存在于分子内部的作用力。它比化学键弱,比范德华力强。当H原子与电负性大、半径较小的原子X以共价键结合时,H原子能够跟另一个电负性大、半径较小的原子Y之间形成氢键。因此,氢键通常用X-H...Y表示,其中X和Y代表电负性大而原子半径较小的非金属原子,如氟、氧、氮等。

图水分子之间形成复健的示意图
当分子间存在氢键时,若要使相应的物质熔化或汽化,由于破坏分子间的氢键需要消耗较多的能量,所以这些物质有较高的熔点和沸点。此外,氢键还会影响物质的溶解性等性质,如乙醇和水能以任意比例互溶。
3.基本要求:
(1)要求配合教学内容有简单的板书设计。
(2)教学过程中要有课堂互动环节。
(3)请在十分钟内完成试讲。
已知
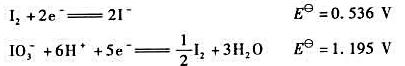
(1)试将上述两个反应的电势-pH图画在同一坐标系中;
(2)试从电势-pH图判断单质I2发生歧化反应生成I-和IO3-,的pH条件,并写出歧化反应的方程式。
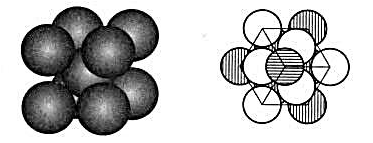
(1)试计算金属晶体中钾原子的空间占有率;
(2)试计算金属晶体中铂原子的空间占有率;
(3)已知铂的相对原子质量为195.08,若金属铂的立方晶胞的边长a=392.3pm,试计算每立方厘米金属铂的质量。
密闭容器中的反应CO(g)+H2O(g)=CO2(g)+H2(g)在750K时其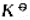 =2.6,试计算:
=2.6,试计算:
(1)当原料气中H2O(g)和CO(g)的物质的量之比为1:1时,CO(g)的转化率为多少?
(2)当原料气中H2O(g)和CO(g)的物质的量之比为4:1时,CO(g)的转化率为多少 ? 说明什么问题?
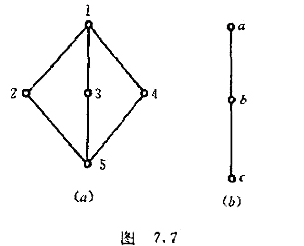
试证明从图7.7(a)的五元素格到(b)的三元素链存在一个映射,凡此映射是保序的,它是否是一个同态?