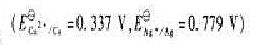题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[单选题]
标准锌电极和标准铜电极组成的原电池,若只增加ZnSO4溶液浓度,其它条件不变,则电池电动势()。
A.减小
B.增加
C.不变
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.减小
B.增加
C.不变
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“标准锌电极和标准铜电极组成的原电池,若只增加ZnSO4溶液浓…”相关的问题
更多“标准锌电极和标准铜电极组成的原电池,若只增加ZnSO4溶液浓…”相关的问题
以Ag/AgC1与铜离子选择性电极组成下列电池饱和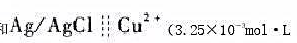
 铜离子选择性电极
铜离子选择性电极
在25℃时,测得电池的电动势为0.124V。若用未知铜活度的溶液取代上述电池中Cu2+(3.25X10-3mo1•L-1)的溶液,测得其电动势为0.086V。计算未知液中pCu(不考虑液接电位)。
A.原电池主要是利用两极的电势差,使电子偏向一方,从而产生电流
B.原电池的电极由两极材料决定,两者相比容易失去电子的一极为负极
C.活泼的一极为负极,另一极则为正极
D.不一定活泼的一极为负极,另一极则为正极,铜铝在浓硝酸中,铜是负极
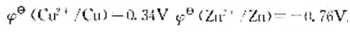 ,求此时原电池的电动势比标准状态时的电动势()
,求此时原电池的电动势比标准状态时的电动势()A.上升0.24V
B.下降0.24V
C.上升0.12V
D.下降0.12V
A.电极电势是指电极与溶液之间的界面电位差,它可由实验测出
B.还原电极电势越高,该电极氧化态物质得到电子的能力越强
C.电极电势只与电极材料有关,与温度无关
D.电极电势就是标准电极电势
某溶液含有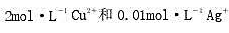 ,若以Pt为电极进行电解。
,若以Pt为电极进行电解。
(1)在阴极上首先析出的是铜还是银?
(2)能否使两种金属离子完全分离?若可以完全分离,阴极电位控制在多少?铜和银在Pt电极上的过电位可忽略不计。