 更多“当放热的可逆反应达到了平衡时,温度升高10℃,则平衡常数会降…”相关的问题
更多“当放热的可逆反应达到了平衡时,温度升高10℃,则平衡常数会降…”相关的问题
已知可逆反应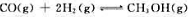 在523K和548K时的标准平衡常数分别为2.3×10-3和5.4×10-4,该可逆反应在一定条件下达到了化学平衡。当升高温度时,化学平衡向()方向移动;加入催化剂后,化学平衡()。
在523K和548K时的标准平衡常数分别为2.3×10-3和5.4×10-4,该可逆反应在一定条件下达到了化学平衡。当升高温度时,化学平衡向()方向移动;加入催化剂后,化学平衡()。
题目来源:1月7日下午山西省大同市面试考题
试讲题目
1.题目:化学平衡
2.内容:
二、化学平衡状态
如果把溶质《不限于固体)在溶液中形成饱和溶被时的状态。称为溶解平衡状态,对于化学反应体系来说,就应当称作化学平衡状态。容解平衡所具有的许多特点,在:化学平衡体系中都可以找到。例如。在反应体系中同时存在着正、道反应两个过程,当这两个过程的速率不相等时,常常只能观购到某个力向的变化。
在一定条件下,当正、逆两个方向的反应速率相等时,反应体系中所有参加反应的物质的质量或浓度可以保持恒定。这时的状态也就是在给定条件下,反应达到了“限度”。对于可逆反应体系来说。我们称之为“化学平衡状态"。这时正、逆变化过程虽然仍在继续,如果不采用特殊的方法或技术,实际观察到的是一种“反应停止了”的表观现象。由此我们可以总结出以下的认识:
1.构成化学平衡体系的基本要求是:反应物和所有产物均处于同一反应体系中,反应条件(如温度、压强等)保持不变。
2.达到化学平衡状态时,体系中所有反应物和生成物的质量(或浓度)保持不变。但是这个体系中的反应并没有停止。只是正、逆反应的速率相等。
我们知道,不同湖度下物质的溶解度不同。那么,t0时达到溶解平衡状态的饱和溶液,当升高或降低温度至t1时,溶解与结晶的速率不再相等。溶解平衡状态被打破,表现为固体溶质继续溶解或析出,直至溶解与结晶的速率再次相等,达到t1下新的溶解平衡状态。
那么化学平衡是否也只有在一定的条件下才能保持?当一个可逆反应达到化学平衡状态后,如果改变浓度,压强。温度等反应条件,平衡状态是否也会发生变化?
有人认为,如果把那些能够进行到底的化学反应体系也看作是可逆性的,亦即相当于正反应的限度接近100%。逆反应的限度几乎等于0的一种情况,就可以把这两类看来似乎迥然不同的反应统一起。不过在定义可逆反应时,有一个必要的前提。那就是,反应物和产物必需同时存在于同一反应体系中,而且在相同条件下,正、逆反应都能够自动进行,不能满足这个前提的化学反应体系,就不能认为是可逆性的。
化学平衡:chemical equilibrium
3.基本要求:
(1)要有适当的情境创设。
(2)教学过程中要有课堂互动环节。
(3)请在十分钟内完成试讲。
反应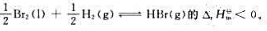 上述可逆反应达到化学平衡后,降低温度时,平衡()移动:缩小容器的体积增大压力时,平衡()加入催化剂时,标准平衡常数()移动;升高温度时,标准平衡常数()。
上述可逆反应达到化学平衡后,降低温度时,平衡()移动:缩小容器的体积增大压力时,平衡()加入催化剂时,标准平衡常数()移动;升高温度时,标准平衡常数()。
A.增大压力
B.增大D的浓度
C.使用催化剂
D.升高温度
可逆反应 达到平衡后,升高温度,平衡向正反应方向移动。这说明()
达到平衡后,升高温度,平衡向正反应方向移动。这说明()
A、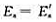
B、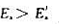
C、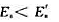
D、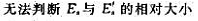
氮化镓(GaN)是第三代半导体材料,具有热导率高、化学稳定性好等性质,在光电领域和高频微波器件应用等方面有广阔的前景。
(1)传统的氮化镓制各方法是采用GaC13与NH3在一定条件下反应。NH3的电子式为()。
(2)Johnson等人首次在1100℃下用液态镓与氨气制得氮化镓固体,该可逆反应每生成1molH2放出10.3kJ热量。其热化学方程式为()。
(3)在恒容密闭容器中,加入一定量的液态镓与氨气发生上述反应,测得反应平衡体系中NH3的体积分数与压强(p)、温度(T)的关系如图所示。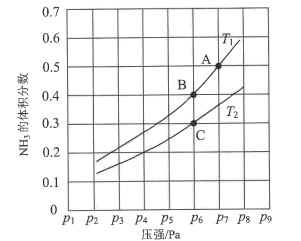 ①下列说法正确的是()(填标号)。
①下列说法正确的是()(填标号)。
a.温度:T1>T2
b.当百分含量ω(NH3)=ω(H2)时,说明该反应处于化学平衡状态
c.A点的反应速率小于C点的反应速率
d.温度恒定为T2,达平衡后再充入氦气(氦气不参与反应),NH3的转化率不变
②既能提高反应速率又能使平衡正向移动的措施有()(写出一条即可)。
③气体分压(p分)=气体总压(p总)×体积分数,用平衡分压代替物质的量浓度也可以表示平衡常数(记作Kp)。在T2时,用含p6的计算式表示C点的()。
(4)如图可表示氮化镓与铜组装成的人工光合系统的工作原理。H+向()(填“左”或“右”)池移动;铜电极上发生反应的电极反应式为()。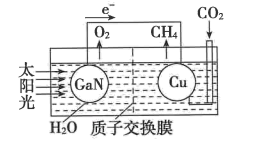
A、增大反应物的分压
B、升高温度
C、加入催化剂
D、增大压力
A.反应物浓度,放热,放热,吸热
B.反应物浓度,吸热,吸热,放热
C.反应的热效应,吸热,放热,吸热
D.反应的热效应,吸热,吸热,放热


 如果结果不匹配,请
如果结果不匹配,请 

















