 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
利用标准摩尔生成吉布斯自由能数据,分析298.15K时,通过以下两组反应制备苯胺的可能性.已知:
利用标准摩尔生成吉布斯自由能数据,分析298.15K时,通过以下两组反应制备苯胺的可能性.
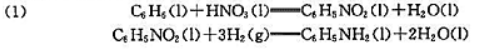
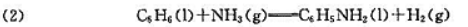
已知:
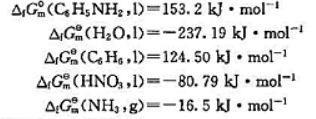
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
利用标准摩尔生成吉布斯自由能数据,分析298.15K时,通过以下两组反应制备苯胺的可能性.
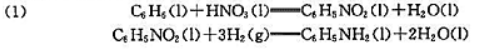
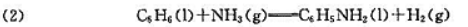
已知:
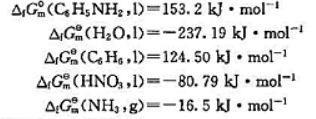
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“利用标准摩尔生成吉布斯自由能数据,分析298.15K时,通过…”相关的问题
更多“利用标准摩尔生成吉布斯自由能数据,分析298.15K时,通过…”相关的问题
应用附录中有关物资的热化学数据,计算25°C时反应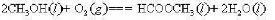 的标准摩尔反应始,要求:
的标准摩尔反应始,要求: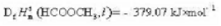
(1)应用25°C的标准摩尔生成焓数据:
(2)应用25°C的标准摩尔燃烧焓数据。
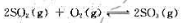
反应达到平衡时,测得混合物中有6.0molSO2(g)。试计算:
(1)该可逆反应在800K时的标准平衡常数和标准摩尔吉布斯自由能变;
(2)SO2在上述条件下的平衡转化率。
植物在光合作用中合成葡萄糖的反应可以近似表示为:
6CO2(g)+6H2O(1)=C6H12O6(s)+6O2(g)
计算反应的标准摩尔吉布斯自由能,判断反应在298K及标准状态下能否自发进行,已知葡萄糖的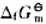 (C6H12O6·s) =-910.5kJ·mol-1。
(C6H12O6·s) =-910.5kJ·mol-1。
利用键能数据估算丙烷的标准摩尔燃烧焓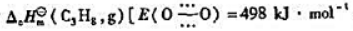 E(C=0)=803KJ.mol-1,其他键能数据查教材上表9-6].
E(C=0)=803KJ.mol-1,其他键能数据查教材上表9-6].
A.升高温度使吉布斯自由能变和和标准吉布斯自由能变均增大
B.升高温度可以使平衡向右移动
C.升高温度可以使平衡常数增大
D.正反应自发时,随着反应进行,N2和H2分压逐渐减小,NH3分压逐渐增大,所以平衡常数Kp逐渐增大
已知25℃时,液态水的标准摩尔生成吉布斯函数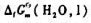 =-237.129kJ·mol-1,饱和蒸气压p''=3.1663kPa.求25℃时水蒸气的标准摩尔生成吉布斯函数.
=-237.129kJ·mol-1,饱和蒸气压p''=3.1663kPa.求25℃时水蒸气的标准摩尔生成吉布斯函数.