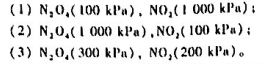题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
已知反应2SO2+O2=2SO3,在1062K时的 =0.955,如果在该温度下,于某一容器中含有SO2
已知反应2SO2+O2=2SO3,在1062K时的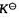 =0.955,如果在该温度下,于某一容器中含有SO2,O2,SO3三种气体,其分压力分别为:p(SO2)=30.4kPa,p(O2)= 60.1kPa, p(SO3)=25.3kPa。试判断反应进行的方向。
=0.955,如果在该温度下,于某一容器中含有SO2,O2,SO3三种气体,其分压力分别为:p(SO2)=30.4kPa,p(O2)= 60.1kPa, p(SO3)=25.3kPa。试判断反应进行的方向。
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知反应2SO2+O2=2SO3,在1062K时的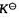 =0.955,如果在该温度下,于某一容器中含有SO2,O2,SO3三种气体,其分压力分别为:p(SO2)=30.4kPa,p(O2)= 60.1kPa, p(SO3)=25.3kPa。试判断反应进行的方向。
=0.955,如果在该温度下,于某一容器中含有SO2,O2,SO3三种气体,其分压力分别为:p(SO2)=30.4kPa,p(O2)= 60.1kPa, p(SO3)=25.3kPa。试判断反应进行的方向。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知反应2SO2+O2=2SO3,在1062K时的 =0.9…”相关的问题
更多“已知反应2SO2+O2=2SO3,在1062K时的 =0.9…”相关的问题
A.路低温度
B.增大压力
C.加入氧气
D.去掉三氧化硫
A.50
B.0.01
C.10
D.无法确定
题目来源:1月7日上午河南省郑州市面试考题
试讲题目
1.题目:硫酸的制备
2.内容:
如果以硫黄为原料制硫酸,你能试着用化学方程式表示制硫酸的反应原理吗?
目前,工业上制硫酸的基本生产原理如下:
1.以硫为原料制备SO2
S(s)+O2(g)═SO2(g)(放热反应)
2.利用催化氧化反应将SO2氧化成SO3
2SO2(g)+O2(g)═(催化剂)2SO3(g)(放热反应)
3.三氧化硫转化为硫酸
SO3(g)+H2O(l)═H2SO4(l)(放热反应)
按照上述反应原理,工业上制硫酸主要分造气、催化氧化和吸收三个阶段。

图1-2硫酸工业流程
在生产中还应考虑许多实际问题,如原料的净化、反应条件及设备的选择、废热的利用等。
已知298.15K时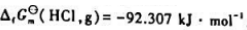 化学反应
化学反应
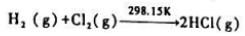
在催化剂的作用下反应速率大大加快时,反应的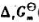 (298.15K)=().
(298.15K)=().
已知四氧化二氮的分解反应如下:

在298.15K时,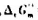 =4.75kJ·mol-1.试判断在此温度及下列条件下,反应进行的方向.
=4.75kJ·mol-1.试判断在此温度及下列条件下,反应进行的方向.