题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知下列电极反应的标准电极电势:(1)计算反应:的KΘ;(2)已知计算反应:的标准平衡常数K卐
已知下列电极反应的标准电极电势:
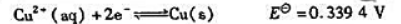
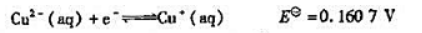
(1)计算反应: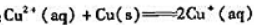 的KΘ;
的KΘ;
(2)已知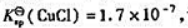 计算反应:
计算反应:
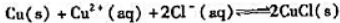 的标准平衡常数KΘ:
的标准平衡常数KΘ:
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知下列电极反应的标准电极电势:
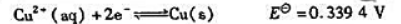
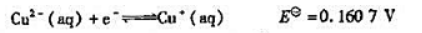
(1)计算反应: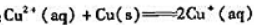 的KΘ;
的KΘ;
(2)已知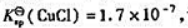 计算反应:
计算反应:
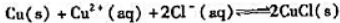 的标准平衡常数KΘ:
的标准平衡常数KΘ:
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知下列电极反应的标准电极电势:(1)计算反应:的KΘ;(2…”相关的问题
更多“已知下列电极反应的标准电极电势:(1)计算反应:的KΘ;(2…”相关的问题
查表写出下列电极反应的标准电极电势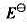 据此回答下列问题:
据此回答下列问题:
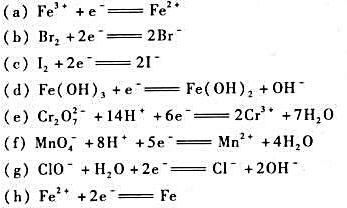
(1)哪些电极反应的电极电势值不受介质的酸碱性影响?
(2)哪种物质是酸性介质中最强的氧化剂?哪种物质是碱性介质中最强的还原剂?
(3)在标准状态下,哪些物质可以将Br-氧化?
(4)在标准状态下,哪些物质可以将Fe3+还原?
(5)降低pH,哪些电极反应的电极电势值升高?
已知电极反应:
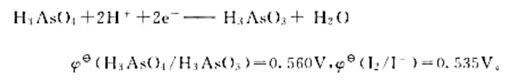
计算下列反应:
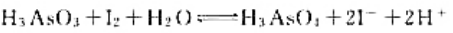
(1)在298K时的平衡常数;
(2)如果pH=7,其他物质浓度均为标准态,反应向什么方向进行?
(3)如果溶液的c(H+)=6.0mol·L-1.其他物质浓度均为标准态.反应向什么方向进行?
将下列化学反应写成两个电极反应,查表求出其电极电势值并计算原电池的电动势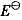 ,再计算电池反应的
,再计算电池反应的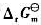 。
。

A.Cl2+2e=2Cl-
B.Sn4++2e=Sn2+
C.2Hg2++2e=Hg22+
D.2H++2e=H2
A.电极电势是指电极与溶液之间的界面电位差,它可由实验测出
B.还原电极电势越高,该电极氧化态物质得到电子的能力越强
C.电极电势只与电极材料有关,与温度无关
D.电极电势就是标准电极电势
已知下列电对的标准电极电势:
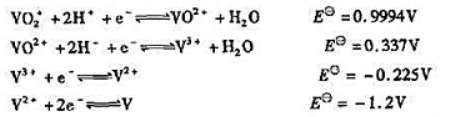
在酸性溶液中分别用1.0mol·L-1Fe2+,1.0mol·L-1Sn2+和Zn还原1.0mol·L-1的VO2+时,最终得到的产物各是什么(不必计算)?
根据标准电极电位数据,判断下列论述是否正确:
(1)在Cl-、Br-、I-溶液中,除I-外,其他离子都能被Fe3+氧化。已知: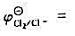

(2)用间接碘量法测定时CuSO4时,Fe3+能氧化I-析出I2,因而干扰CuSO4的测定,加入NH4HF2可消除此干扰。已知: