 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
25℃下某电极反应的J0为5×10-3安培/米2。在恒电位极化下的过电位为-0.199V时,稳态电流密度为多少?应用快速开关切断恒电位仪,然后对电极施加恒定的阴极电流密度0.205安培/米2,问达新稳态下的过电位是多少?假定β=0.5。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“25℃下某电极反应的J0为5×10-3安培/米2。在恒电位极…”相关的问题
更多“25℃下某电极反应的J0为5×10-3安培/米2。在恒电位极…”相关的问题
丙烷燃料电池的电极反应为
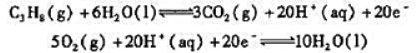
(1)指出正极反应和负极反应;
(2)写出电池反应方程式;
(3)计算25℃下丙烷燃料电池的标准电动势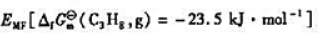
在25℃时测定某一电极反应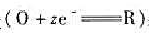 得下列数据:
得下列数据:

平均极限扩散电流为3.24mA,求:
(1)电极反应的转移电子数;
(2)电极反应是否可逆;
(3)假定氧化态和还原态的活度系数和扩散系数相等,计算氧化还原体系的标准电位(相对于SCE)。
甲烷燃烧过程可设计成燃料电池.当电解质为酸性溶液时,电极反应和电池反应分别为
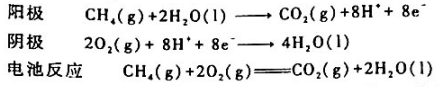
已知,25°C时有关物质的标准摩尔生成吉布斯函数 为
为
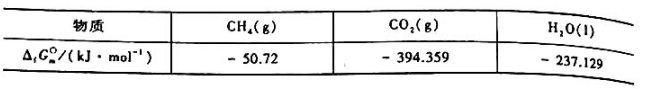
计算25°C时该电池的标准电动势.
某股票5年来的增长率分别为:15%、32%、5%、3%和2%,试求其年平均增长率()。
A.10.86%
B.11.26%
C.11.40%
D.12.58% 资料:假设某股票市场遭遇牛市、熊市、正常市的概率分别为三分之一,有三只股票 X、Y、Z,在牛市下,X的收产益率为20%,Y的收益率为15%,Z的收益率为25%,在正常市下,X的收益率为10%,Y的收益率为5%,z的收益率为5%,在熊市下,X的收益率为-5%,Y的收益率为-10%,z的收益率为-15%。回答4~10题:
已知铅酸蓄电池
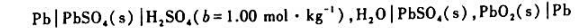
在25°C时的电动势E=1.9283V,Eθ=2.0501V.该电池的电池反应为
Pb(s)+PbO2(s)+2SO42-+4H+→2PbSO4(s)+2H2O
(1)请写出该电池的电极反应;
(2)计算该电池中硫酸溶液的活度a、平均离子活度az及平均离子活度因子γz;
(3) 已知该电池的温度系数为5.664x10-5V·K-1,计算电池反应的ΔrGm,ΔrSm,ΔrHm,
及可逆热Qr,m.
用KMnO4标准溶液滴定Fe2+的反应为:

试计算:①该反应的平衡常数;②为使反应完全定量进行(Fe2+≤10-3[Fe3+]),所需的最低[H+]是多少?(已知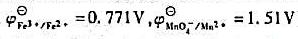 )
)