 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在恒容密闭容器中发生反应2NO2⇌2NO+O2,,下列所述可以说明反应达到平衡状态的是()①单位时间内生成n molO2的同时生成2n molNO2 ②单位时间内生成n molO2的同时生成2n molNO ③混合气体的颜色不再改变 ④混合气体的密度不再改变
A.①③
B.②④
C.①③④
D.①②③④
 答案
答案
A、①③
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.①③
B.②④
C.①③④
D.①②③④
 答案
答案
A、①③
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“在恒容密闭容器中发生反应2NO2⇌2NO+O2,,下列所述可…”相关的问题
更多“在恒容密闭容器中发生反应2NO2⇌2NO+O2,,下列所述可…”相关的问题
A.平衡后升高温度,容器中气体颜色加深
B.每消耗44.8LNO2,生成N2O4的分子数一定为NA
C.该容器中气体质量为46g时,原子总数为3NA
D.若N2O4分子数增加0.5NA,则放出0.5akJ的热量
A.增大容器体积
B.体积不变,充入N2使压强增大
C.体积不变,充入He使压强增大
D.压强不变,充入He使体积增大
A.气体总质量不变
B.混合气体密度不变
C.反应物B的浓度不变
D.混合气体平均相对分子质量不再改变
g)和H2O(l)。过程放热401.727kJ。求
已知NO与H2可进行如下化学反应:
2NO(g)+2H2(g)→N2(g)+2H2O(g)
在一定温度下,某密闭容器中等摩尔比的NO与H2混合物在不同初始压力下的半衰期如下:

求反应的总级数n.
A.容器内压强不再变化,说明反应达到平衡状态
B.当c(SO2):c(O2)=2:1表明反应达到平衡状态
C.加入合适的催化剂可显著增大反应速率,提高SO2的转化率
D.达到平衡状态时,相同时间内,每消耗2molSO3的同时生成1molO2
A.CO(g)+Cl2(g)→COCl2(g)
B.2NO2(g)→NO(g)+1/2O2(g)
C.N2(g)+O2(g)→2NO(g)
D.NH4HS(s)→NH3(g)+H2S(g)
氮化镓(GaN)是第三代半导体材料,具有热导率高、化学稳定性好等性质,在光电领域和高频微波器件应用等方面有广阔的前景。
(1)传统的氮化镓制各方法是采用GaC13与NH3在一定条件下反应。NH3的电子式为()。
(2)Johnson等人首次在1100℃下用液态镓与氨气制得氮化镓固体,该可逆反应每生成1molH2放出10.3kJ热量。其热化学方程式为()。
(3)在恒容密闭容器中,加入一定量的液态镓与氨气发生上述反应,测得反应平衡体系中NH3的体积分数与压强(p)、温度(T)的关系如图所示。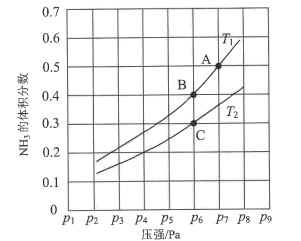 ①下列说法正确的是()(填标号)。
①下列说法正确的是()(填标号)。
a.温度:T1>T2
b.当百分含量ω(NH3)=ω(H2)时,说明该反应处于化学平衡状态
c.A点的反应速率小于C点的反应速率
d.温度恒定为T2,达平衡后再充入氦气(氦气不参与反应),NH3的转化率不变
②既能提高反应速率又能使平衡正向移动的措施有()(写出一条即可)。
③气体分压(p分)=气体总压(p总)×体积分数,用平衡分压代替物质的量浓度也可以表示平衡常数(记作Kp)。在T2时,用含p6的计算式表示C点的()。
(4)如图可表示氮化镓与铜组装成的人工光合系统的工作原理。H+向()(填“左”或“右”)池移动;铜电极上发生反应的电极反应式为()。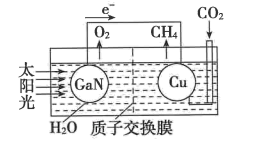
A.升温加压
B.升温降压
C.降温加压
D.降温降压