题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
下列能够检验出KI溶液中含有Br-的实验是()
A.加入足量的新制氯水,溶液变色则有Br-
B.加入酸性KMnO4溶液,观察溶液颜色是否褪去,褪色则含有Br-
C.加入少量的碘水,再加入CCl4振荡,有机层有色,则有Br-
D.加入足量FeCl3溶液,用CCl4萃取后,在水层中加入氯水,溶液呈橙色,则含Br-
 答案
答案
D、加入足量FeCl3溶液,用CCl4萃取后,在水层中加入氯水,溶液呈橙色,则含Br-
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.加入足量的新制氯水,溶液变色则有Br-
B.加入酸性KMnO4溶液,观察溶液颜色是否褪去,褪色则含有Br-
C.加入少量的碘水,再加入CCl4振荡,有机层有色,则有Br-
D.加入足量FeCl3溶液,用CCl4萃取后,在水层中加入氯水,溶液呈橙色,则含Br-
 答案
答案
D、加入足量FeCl3溶液,用CCl4萃取后,在水层中加入氯水,溶液呈橙色,则含Br-
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“下列能够检验出KI溶液中含有Br-的实验是()”相关的问题
更多“下列能够检验出KI溶液中含有Br-的实验是()”相关的问题
A.上述实验证明氧化性:MnO4— > Cl2 > Fe3+ > I2
B.上述实验中共发生了两个氧化—还原反应
C.实验①生成的气体不能使湿润的淀粉KI试纸变蓝
D.实验②可以证明Fe2+既有氧化性又有还原性
A.用CO2鉴别NaOH溶液和Ca(OH)2溶液
B.用水鉴别硝酸铵固体和氢氧化钠固体
C.用无色酚酞试液检验NaOH溶液是否变质
D.用过滤的方法从H2O2溶液制氧气的残余物中分离出MnO2
说明用下述方法进行测定是否会引人误差,如有误差则指出偏高还是偏低?
(1)吸取NaCl+H2SO4试液后,马上以摩尔法测Cl-;
(2)中性溶液中用摩尔法测定Br-;
(3)用摩尔法测定pH~8的KI溶液中的I-;
(4)用摩尔法测定Cl-,但配制的K2CrO4指示剂溶液浓度过稀;
(5)用佛尔哈德法测定Cl-,但没有加硝基苯.
A.在溶液中加KSCN溶液显红色,证明原溶液中有Fe3+,无Fe2+
B.气体通过无水CuSO4,粉末变蓝,证明该气体中含有水蒸气
C.灼烧白色粉末,火焰呈黄色,证明原粉末中有Na+,无K+
D.将气体通入澄清石灰水,溶液变浑浊,证明原气体是CO2
A.1.0 mol·L-1的KNO3溶液:H+、Fe2+、Cl-、SO42-
B.酸性溶液:NH4+、Ba2+、AlO2-、Cl-
C.pH=12的溶液:K+、Na+、CH3COO-、Br-
D.与铝反应产生大量氢气的溶液:Na+、K+、CO32-、NO3-
根据标准电极电位数据,判断下列论述是否正确:
(1)在Cl-、Br-、I-溶液中,除I-外,其他离子都能被Fe3+氧化。已知: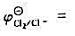

(2)用间接碘量法测定时CuSO4时,Fe3+能氧化I-析出I2,因而干扰CuSO4的测定,加入NH4HF2可消除此干扰。已知: