 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
若溶液的pH=11.00,游离CN-的浓度为1.0*10-2mol.L-1计算HgY络合物的 值。已
若溶液的pH=11.00,游离CN-的浓度为1.0*10-2mol.L-1计算HgY络合物的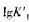 值。已知Hg2+-CN-络合物的逐级形成常数
值。已知Hg2+-CN-络合物的逐级形成常数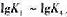 分别为:18.00,16.70,3.83和2.98.
分别为:18.00,16.70,3.83和2.98.
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
若溶液的pH=11.00,游离CN-的浓度为1.0*10-2mol.L-1计算HgY络合物的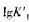 值。已知Hg2+-CN-络合物的逐级形成常数
值。已知Hg2+-CN-络合物的逐级形成常数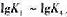 分别为:18.00,16.70,3.83和2.98.
分别为:18.00,16.70,3.83和2.98.
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“若溶液的pH=11.00,游离CN-的浓度为1.0*10-2…”相关的问题
更多“若溶液的pH=11.00,游离CN-的浓度为1.0*10-2…”相关的问题
A.2.56mol·L-1
B.1.28mol·L-1
C.0.098mol·L-1
D.0.049mol·L-1
向0.10mol·dm-3草酸溶液中滴加NaOH溶液至pH=6.00,试求溶液中H2C2O4,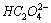 和
和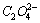 的浓度。已知H2C2O4的K1=5.4×10-2,K2=5.4×10-5。
的浓度。已知H2C2O4的K1=5.4×10-2,K2=5.4×10-5。
A.用标准缓冲溶液pH为6.86和9.18的校正酸度计
B.用NaOH溶液准确地中和样品中的游离酸
C.应加入10mL甲酸溶液
D.用NaOH标准溶液滴至pH为9.20
A.NaOH中和游离酸的操作应在加入沸水后进行
B.加入过量KCl、KF以提高K2SiF6溶解度
C.可溶性的硅酸盐中加入HF使生成K2SiF6沉淀
D.试样在浓HCl溶液中溶解
已知M(NH3)42+的 为2.0、5.0、7.0、10.0; M(OH)42+的
为2.0、5.0、7.0、10.0; M(OH)42+的 为4.0、8.0、 14.0、15.0.在浓度为0.10 mol.L-1的M2+溶液中,滴加氨水至溶液中的游离NH3度为0.010mol.L-1, pH=9.0.试问溶液中的主要存在形式是哪一种? 浓度为多大?若将M2+溶液用NaOH和氨水调节至pH=13.0且游离NH3浓度为0.010mol.L-1则上述溶液中的主要存在形式是什么?浓度又为多少?
为4.0、8.0、 14.0、15.0.在浓度为0.10 mol.L-1的M2+溶液中,滴加氨水至溶液中的游离NH3度为0.010mol.L-1, pH=9.0.试问溶液中的主要存在形式是哪一种? 浓度为多大?若将M2+溶液用NaOH和氨水调节至pH=13.0且游离NH3浓度为0.010mol.L-1则上述溶液中的主要存在形式是什么?浓度又为多少?