 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
当两对电子转移数分别为1和2,为使反应完全程度达到99.9%,两电对的条件电位差至少应大于()。
A.0.09V
B.0.18V
C.0.24V
D.0.27V
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.0.09V
B.0.18V
C.0.24V
D.0.27V
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“当两对电子转移数分别为1和2,为使反应完全程度达到99.9%…”相关的问题
更多“当两对电子转移数分别为1和2,为使反应完全程度达到99.9%…”相关的问题
在25℃时测定某一电极反应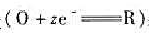 得下列数据:
得下列数据:

平均极限扩散电流为3.24mA,求:
(1)电极反应的转移电子数;
(2)电极反应是否可逆;
(3)假定氧化态和还原态的活度系数和扩散系数相等,计算氧化还原体系的标准电位(相对于SCE)。
车床的传动装置如图7-7所示。已知各齿轮的齿数分别为: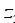 1=40,
1=40,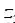 2=84,
2=84,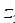 3=28,
3=28,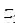 4=80;带动刀具的丝杠的螺距为h4=12mm。求车刀切削工件的螺距h1。
4=80;带动刀具的丝杠的螺距为h4=12mm。求车刀切削工件的螺距h1。
题目来源:1月6日上午山东省临沂市面试考题
试讲题目
1.题目:原电池
2.内容:
要想使氧化还原反应释放的能量直接转变为电能,就要设计一种装置,使氧化反应和还原反应分别在两个不同的区域进行,并使其间的电子转移,在一定条件下形成电流。为了使用方便,还需要把可产生的电能以化学能的形式储存起来。化学电池就是这样一种装置。这种装置可以将氧化还原反应体系的能量储存起来,类似于水库的蓄存水能。
实验2-4
将锌片和铜片用导线连接(导线中间接入一个电流表),平行插入盛有稀硫酸的烧杯中(如图2-9),观察现象。

学与问
根据你所了解的电学知识,你知道电子是怎样流动的吗?你如何判定装置的正、负板?由于锌和铜的活动性不同,锌容易失去电子,被氧化成Zn2+进入溶液,电子由锌片通过导线流向铜片,溶液中的H+从铜片获得电子被还原成氢原子,氢原子再结合成氢分子从铜片上逸出。这一变化过程可以表示如下:
锌片:Zn-2e-=Zn2+(氧化反应)
铜片:2H++2e-=H2↑(还原反应)
我们把这种将化学能转为电能的装置叫做原电池,最早的化学电池就是根据原电池原理制成的。
3.基本要求:
(1)试讲过程中要设置互动环节。
(2)试讲要讲清原理与实验。
(3)试讲时要有适当的板书设计。
答辩题目
1.化学教学提问的基本要求是什么?
2.原电池反应时锌这端也会有气泡产生,是什么原因?怎样避免?
A.Na原子失去电子,化合价升为+1
B.Na原子在此反应中为还原剂
C.Cl原子在反应中得到电子,为氧化剂
D.此反应中化合价变化,电子没有转移
A.0.09V
B.0.18V
C.0.27V
D.0.36V
问题描述:假设有来自n个不同单位的代表参加一次国际会议.铄个单位的代表数分别为ri(i=1,2,...,n).会议餐厅共有m张餐桌,每张餐桌可容纳ci(i=1,2,...,m)个代表就餐.为了使代表们充分交流,希望从同一个单位来的代表不在同一个餐桌就餐.试设计一个算法,给出满足要求的代表就餐方案.
算法设计:对于给定的代表数和餐桌数以及餐桌容量,计算满足要求的代表就餐方案.
数据输入:由文件input.txt提供输入数据.文件第1行有2个正整数m和n,m表示餐桌数,n表示单位数(1≤m≤150,1≤n≤270).文件第2行有m个正整数,分别表示每个单位的代表数.文件第3行有n个正整数,分别表示每个餐桌的容量.
结果输出:将代表就餐方案输出到文件output.txt如果问题有解,在文件第1行输出1,否则输出0.接下来的m行给出每个单位代表的就餐桌号.如果有多个满足要求的方案,只要输出一个方案.
