 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
有一标准Fe3+溶液,浓度为6μg/ml,其吸光度为0.304,而试样溶液在同一条件下测得吸光度为0.510,求试样溶液中Fe3+的含量(mg/L)。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“有一标准Fe3+溶液,浓度为6μg/ml,其吸光度为0.30…”相关的问题
更多“有一标准Fe3+溶液,浓度为6μg/ml,其吸光度为0.30…”相关的问题
A.用10 mL量筒量取7.36 mL NaOH溶液
B.用托盘天平称取6.85 g食盐
C.用标准盐酸滴定未知浓度的NaOH溶液,用去盐酸21.10 mL
D.用广泛pH试纸测得某溶液pH为5
,然后用 0.03000 mol·L-1 K2Cr2O7溶液滴定,用去25.00 mL。计算试样中FeO和Al2O3的质量分数
用火焰原子吸收分光光度法测土壤中铜。称取风干过筛土样1.00 g(含水8.20%),经消解后定容至50.0 mL,用标准曲线法测得此溶液铜的浓度为0.700 mg/L,求被测土壤中铜的含量。
A.0.1mg/mL~10mg/mL 4℃ 3个月
B.0.5mg/mL~1mg/mL 4℃6个月
C.0.1mg/mL~10mg/mL 4℃ 6个月
D.0.5mg/mL~1mg/mL 4℃ 3个月
随着工业的迅速发展,产生的废水对水体的污染也日趋严重。通过控制溶液的pH对工业废水中的金属离子进行别离是实际工作中经常使用的方法。下表是常温下金属氢氧化物的Ksp(沉淀溶解平衡常数)和金属离子在某浓度下开始沉淀所需的pH(表中浓度为相应pH时溶液中有关金属离子产生沉淀的最小浓度;当溶液中金属离子浓度小于10-5mol•L-1时通常认为该离子沉淀完全)。 问题一、某厂排出的废水中含有Cu2+和Fe3+,测得其浓度均小于0.1mol•L-l。为除去其中的Fe3+,回收铜,需控制的pH范围是()。
问题一、某厂排出的废水中含有Cu2+和Fe3+,测得其浓度均小于0.1mol•L-l。为除去其中的Fe3+,回收铜,需控制的pH范围是()。
问题二、为了处理含有Cr2O72-酸性溶液的工业废水,采用如下方法:向废水中加人适量NaCl,以Fe为电极进行电解,经过一段时间,有Cr(OH)3和Fe(OH)3沉淀生成排出,从而使废水中铬含量低于排放标准
①Cr2O72-转变为Cr3+的离子方程式为()。
②pH对废水中Cr2072-去除率的影响如右图。你认为电解过程中溶液的pH取值在()范围内对降低废水中的铬含量最有利,请说明理由:()。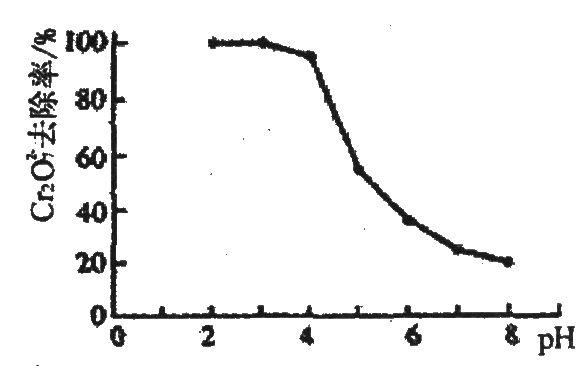
问题三、沉淀转化在生产中也有重要应用。例如,用Na2C03溶液可以将锅炉水垢中的CaS04转化为较疏松而易清除的CaC03,该沉淀转化到达平衡时,其平衡常数K=()。(已知Ksp(CaS04)=9.1x10-6,Ksp(CaC03)=2.8x10-9)