 更多“最外层只有1个电子的元素一定不是非金属元素。()”相关的问题
更多“最外层只有1个电子的元素一定不是非金属元素。()”相关的问题
第6题
已知M2+离子3d轨道中有5个d电子,请推出:(1)M原子的核外电子排布式;(2)M原子的最外层和最高能级组中电子数;(3)M元素在周期表中的位置。
已知M2+离子3d轨道中有5个d电子,请推出:(1)M原子的核外电子排布式;(2)M原子的最外层和最高能级组中电子数;(3)M元素在周期表中的位置。
点击查看答案
此题为判断题(对,错)。
第9题
题目来源:1月6日上午湖南省长沙市面试考题试讲题目1.题目:钠的性质2.内容:金属钠(sodium)的化学
题目来源:1月6日上午湖南省长沙市面试考题
试讲题目
1.题目:钠的性质
2.内容:
金属钠(sodium)的化学性质很活泼,在化学反应中,钠原子很容易失去最外层的一个电子,形成钠离子
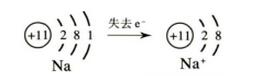
钠离子的形成
1.观察下列实验,并将观察到的现象及所得结论填入表2-3。
【实验1】取一小块金属钠,用滤纸吸干表面的煤油,用刀切去一端的表层,观察表面的颜色;将其放置在空气中,观察表面颜色的变化。
【实验2】将一小块金属钠放在石棉网上加热,观察实验现象。
【实验3】向一只盛有水的小烧杯中滴加几滴酚酞溶液,然后投入一小块(约绿豆粒般大小)金属钠,观察实验现象。
表2-3钠的性质实验

2.根据上述反应中钠元素化合价的变化情况,总结钠的性质。
观察与思考
钠是一种银白色金属,质软,密度为0.97g·cm-3,熔点为97.8℃。
钠单质能够与许多非金属单质、水等物质发生反应,反应中钠失去电子,表现出还原性。
2Na+H2O==2NaOH+H2↑
金属钠露置在空气中与氧气反应,生成白色的氧化钠;钠在空气中燃烧,生成淡黄色的过氧化钠。因此,实验室常将钠保存在煤油中。
4Na+O2==2Na2O
2Na+O2==(点燃)Na2O2
3.基本要求:
(1)让学生了解钠的物理化学性质,尤其是要掌握钠与水的反应。
(2)教学过程中若需要实验或者教具进行语言模拟演示即可。
(3)要求配合教学内容有适当板书设计。
(4)请在10分钟内完成试讲。
答辩题目
1.请你说明这堂课的设计思路?
2.如果金属钠燃烧,应该如何灭火?


 如果结果不匹配,请
如果结果不匹配,请 

















