 更多“已知M2+离子核外有n个电子,则该原子的原子核内质子数为()”相关的问题
更多“已知M2+离子核外有n个电子,则该原子的原子核内质子数为()”相关的问题
第1题
某元素的一种粒子核内有11个质子,核外有11个电子,下列说法错误的是()
A.该粒子属于原子
B.该元素在化合物中显+1价
C.该元素的一个离子含有11个电子
D.该元素的原子在化学反应中容易失去电子
第2题
已知M2+离子3d轨道中有5个d电子,请推出:(1)M原子的核外电子排布式;(2)M原子的最外层和最高能级组中电子数;(3)M元素在周期表中的位置。
已知M2+离子3d轨道中有5个d电子,请推出:(1)M原子的核外电子排布式;(2)M原子的最外层和最高能级组中电子数;(3)M元素在周期表中的位置。
点击查看答案
此题为判断题(对,错)。
第3题
写出Li2+离子的方程,说明该方程中各符号及各项的意义;写出Li2+离子Is态的波函数并计
写出Li2+离子的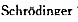 方程,说明该方程中各符号及各项的意义;写出Li2+离子Is态的波函数并计算:
方程,说明该方程中各符号及各项的意义;写出Li2+离子Is态的波函数并计算:
(1)Is电子径向分布最大值离核的距离;
(2)Is电子离核的平均距离;
(3)Is电子概率密度最大处离核距离;
(4)比较Li2+离子的2s和2p态能量的高低;
(5)Li原子的第一电离能(按Slater屏蔽常数算有效核电荷)
第6题
本题通过两个箱中粒子模型的应用实例进行运算:(1)将KCl晶体放置在金属钾蒸气中加热,K原子受辐射
本题通过两个箱中粒子模型的应用实例进行运算:
(1)将KCl晶体放置在金属钾蒸气中加热,K原子受辐射而电离,K→K++e-。K+扩散进入晶体,使晶体的K+离子数目多于Cl-离子数目,晶体的组成变为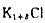 ,为了保持化合物的电中性,电子e-进入负离子的空位代替Cl-,形成
,为了保持化合物的电中性,电子e-进入负离子的空位代替Cl-,形成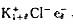 ,晶体显紫红色,这种晶体缺陷结构称色中心。已知Cl-离子半径为181pm,将电子e-看作处于立方体对角线(长为1.73×362pm)作一维势箱运动。试分别求该电子由HOMO→LUMO激发所需的能量以及由LUMO→HOMO所故出光的波长。
,晶体显紫红色,这种晶体缺陷结构称色中心。已知Cl-离子半径为181pm,将电子e-看作处于立方体对角线(长为1.73×362pm)作一维势箱运动。试分别求该电子由HOMO→LUMO激发所需的能量以及由LUMO→HOMO所故出光的波长。
(2)金属钾的摩尔体积室温时为45.36cm3mol-1,试计算它的Fermi能级(EF),分别以J和eV表示,并和实验测定值2.14eV比较。
第9题
已知N原子最外层一未成对电子的四个量子数为(210,1/2),则另两个未成对电子的量子数表达正确的是:()。
A.210(-1/2),211(-1/2)
B.211(-1/2),21-1(-1/2)
C.21-1(1/2),21-1(-1/2)
D.211(1/2),21-1(1/2)
第10题
已知某元素基态原子的电子分布是1s22s22p63s23p63d104s24p1,请回答:(1)该元素的原子序数是多少?(2)该元索属第几周期?第几族?是主族元素还是过渡元素?


 如果结果不匹配,请
如果结果不匹配,请 

















