 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[单选题]
25℃时,已知NH4+的pKa=9.24,则NH3的pKb为()。
A.2.20
B.4.76
C.7.00
D.14.00
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.2.20
B.4.76
C.7.00
D.14.00
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“25℃时,已知NH4+的pKa=9.24,则NH3的pKb为…”相关的问题
更多“25℃时,已知NH4+的pKa=9.24,则NH3的pKb为…”相关的问题
已知25℃时的下列数据:

求110℃时Ag2CO3(s)的分解式.设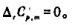
25℃时测得下列电池的电动势为0.622V,求配合物Ag(CN)2-的稳定常数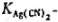 。(已知
。(已知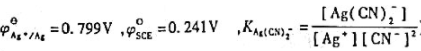 )
)
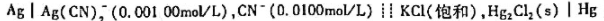
已知25℃时Hg(l)的摩尔体积Vm=1.482x10-5m3·mol-1,体膨胀系数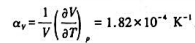 .恒温25℃时将1molHg(l)由100kPa加压到1100kPa,假设此过程Hg的体积变化可忽略不计,则过程的ΔS=()J·K-1.
.恒温25℃时将1molHg(l)由100kPa加压到1100kPa,假设此过程Hg的体积变化可忽略不计,则过程的ΔS=()J·K-1.
已知25℃时,液态水的标准摩尔生成吉布斯函数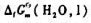 =-237.129kJ·mol-1,饱和蒸气压p''=3.1663kPa.求25℃时水蒸气的标准摩尔生成吉布斯函数.
=-237.129kJ·mol-1,饱和蒸气压p''=3.1663kPa.求25℃时水蒸气的标准摩尔生成吉布斯函数.
已知25℃时AgCl(s);水溶液中Ag+,CI-的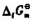 分别为-109.789kJ·mol-1,
分别为-109.789kJ·mol-1,
77.107kJ·mol-1和-131.228kJ·mol-1.求25℃下AgCl(s)在水溶液的标准溶度积Kθ及溶解度s.
甲烷燃烧过程可设计成燃料电池.当电解质为酸性溶液时,电极反应和电池反应分别为
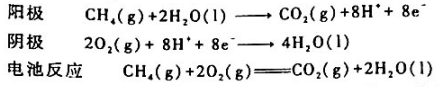
已知,25°C时有关物质的标准摩尔生成吉布斯函数 为
为
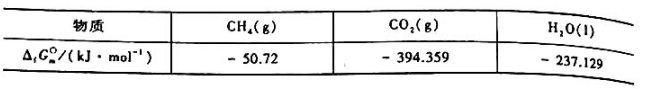
计算25°C时该电池的标准电动势.
已知25°C时AgCl(s).水溶液中Ag+,CI-的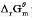 分别为-109.789kJ/mol,77.107kJ/mol和-131.22kJ/mol.求25°C下AgCl(s)在水溶液中的标准溶度积K及溶解度s。
分别为-109.789kJ/mol,77.107kJ/mol和-131.22kJ/mol.求25°C下AgCl(s)在水溶液中的标准溶度积K及溶解度s。