 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
在常温常压下电解(cu+)=1mol·dm-3的硫酸溶液,阳极放出O2(105Pa),阴极
在常温常压下电解(cu+)=1mol·dm-3的硫酸溶液,阳极放出O2(105Pa),阴极
放出H2(105Pa),利用
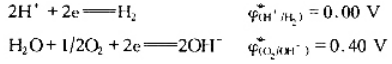
计算理论分解电压,实际分解电压将比理论值大还是小?为什么?若0.10mol·dm-3的NaOH代替硫酸,分解电压为多少?
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
放出H2(105Pa),利用
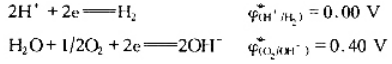
计算理论分解电压,实际分解电压将比理论值大还是小?为什么?若0.10mol·dm-3的NaOH代替硫酸,分解电压为多少?
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“在常温常压下电解(cu+)=1mol·dm-3的硫酸溶液,阳…”相关的问题
更多“在常温常压下电解(cu+)=1mol·dm-3的硫酸溶液,阳…”相关的问题
A.当 x≤4时,常温常压下均为气体
B.y一定是偶数
C.分别完全燃烧1mol,消耗 O₂为 (x+y/4)mol
D.在密闭容器中完全燃烧,120℃时测得的压强一定比燃烧前大
A.常温常压下,4.4gCO2气体中含有的质子数为2.2NA
B.0.1molNa2O2与水充分反应转移的电子数目为0.2NA
C.1mol熔融NaHSO4电离出的阴、阳离子总数目为3NA
D.1mol甲酸中含有共用电子对的数目为4NA