 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
下列实际应用中,与中和反应原理无关的是()
A.用稀盐酸除铁锈
B.用熟石灰改良酸性土壤
C.用硫酸处理印刷厂呈碱性的废水
D.用肥皂水涂在被蚊虫叮咬的皮肤上止痒
 答案
答案
A、用稀盐酸除铁锈
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.用稀盐酸除铁锈
B.用熟石灰改良酸性土壤
C.用硫酸处理印刷厂呈碱性的废水
D.用肥皂水涂在被蚊虫叮咬的皮肤上止痒
 答案
答案
A、用稀盐酸除铁锈
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“下列实际应用中,与中和反应原理无关的是()”相关的问题
更多“下列实际应用中,与中和反应原理无关的是()”相关的问题
A.①②
B.②③
C.①④
D.③④
电解工作原理的实际应用非常广泛。
(1)请画出铜棒镀银的简易装置设计图()。(实验可选用品:铜棒,银片,石墨棒,硫酸铜溶液,硝酸银溶液,导线,电源,烧杯)。
(2)工业上为了处理含有Cr2O12-的酸性工业废水,采用下面的处理方法:往工业废水中加入适量NaCl,以铁为电极进行电解,经过一段时间,有Cr(OH)3和Fe(OH)3沉淀生成,工业废水中铬元素的含量可低于排放标准。关于上述方法,下列说法错误的是()(填字母)。
A、阳极反应:Fe-2e-=Fe2+
B、阴极反应:2H++2e-=H2↑
C、在电解过程中工业废水由酸性变为碱性
D、可以将铁电极改为石墨电极
(3)某同学设计了如图装置进行以下电化学实验。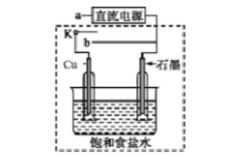 ①当开关K与a连接时,两极均有气泡产生,则阴极为()电极。
①当开关K与a连接时,两极均有气泡产生,则阴极为()电极。
②一段时间后,使开关K与a断开,与b连接时,虚线框内的装置可称为()。请写出此时Cu电极上的电极反应()。
(4)某溶液中含有的离子如下表: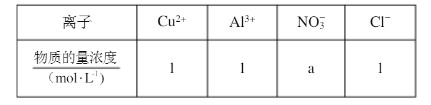 用惰性电极电解该溶液,当电路中有3mole-通过时(忽略电解时溶液体积变化及电极产物可能存在的溶解现象),下列说法正确的是()(填字母)。
用惰性电极电解该溶液,当电路中有3mole-通过时(忽略电解时溶液体积变化及电极产物可能存在的溶解现象),下列说法正确的是()(填字母)。
A、电解后溶液呈酸性
B、a=3
C、阳极生成1.5molCl2
D、阴极析出的金属是铜与铝
B.中和清洗的目的是通过使用碱性稀溶液浸泡和冲洗奥氏体不锈钢金属表面,防止亚硫酸和连多硫酸的生成,或将已经生成的亚硫酸和连多硫酸中和,来达到保护的目的
C.对奥氏体不锈钢还要注意氯化物应力腐蚀裂纹的问题,氯化物应力腐蚀通常是穿晶裂纹
D.奥氏体不锈钢对氯化物的敏感性,与氯化物浓度和温度成正比,在正常的停工期间,一般不会发生氯化物应力腐蚀裂纹。但在高温状态下,由于氯化物的浓缩,就有可能产生应力腐蚀裂纹。因此,在中和清洗的整个过程中,要求化学品、配制用水、配制的中和清洗液中氯化物的含量应在50ppm以下。并注意检修奥氏体不锈钢设备和管道时不要有氯化物渗透吸附,清洗过某一独立系统的中和清洗液,不应再用来清洗另一独立系统
A.粉丝吸引应遵循:群成员有相同的身份或者兴趣爱好;有类似的目标和需求;有情感,价值的联系等原则。
B.根据“鱼塘原理”中’找鱼塘‘原则,运营可以通过深度分析粉丝画像,来精准找鱼。
C.根据“鱼塘原理”中’放鱼饵‘原则,运营可以为直播做更精细化的内容细分与时段安排。
D.根据“鱼塘原理”中’鱼生鱼‘原则,运营可以私下联系粉丝发展其成为店铺淘客。
50ml0.50mol/L盐酸和50ml0.55mol/LNaOH溶液在如下图所示的装置中进行中和反应,通过测定反应过程中所放出的热量可计算中和热,回答下列问题: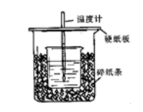 实验中改用60ml0.50mol/L盐酸跟50ml0.55mol/LNaOH溶液进行反应,与上述实验相比,所放放出的热量();填“相等”“不相等”。所求中和热();填“相等”“不相等”。
实验中改用60ml0.50mol/L盐酸跟50ml0.55mol/LNaOH溶液进行反应,与上述实验相比,所放放出的热量();填“相等”“不相等”。所求中和热();填“相等”“不相等”。
A.pH相等的两溶液中:c(CH3COOˉ)=c(Clˉ)
B.分别中和pH相等、体积相等的两溶液,所需NaOH的物质的量相同
C.相同浓度的两溶液,分别与金属镁反应,反应速率相同
D.相同浓度的两溶液,分别与NaOH固体反应后呈中性的溶液中(忽略体积变化):c(CH3COOˉ)=c(Clˉ)
A.NH4HCO3==NH3↑+CO2↑+H2O (分解反应)
B.CuO+H2SO4==CuSO4+H2O (中和反应)
C.2Na+2H2O==2NaOH+H2↑ (置换反应)
D.CaO+H2O==Ca(OH)2 (化合反应)