 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
下列说法正确的是()
A.往某样品溶液中滴加硝酸银溶液,立即出现白色沉淀,则该溶液中含Cl-
B.1molMnO2 与含4molHCl的浓盐酸充分反应,能收集到标况下Cl2 小于 22.4L
C.可以用澄清石灰水来吸收含Cl2的尾气
D.84消毒液可以和洁厕剂混合使用
 答案
答案
B、1molMnO2 与含4molHCl的浓盐酸充分反应,能收集到标况下Cl2 小于 22.4L
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
A.往某样品溶液中滴加硝酸银溶液,立即出现白色沉淀,则该溶液中含Cl-
B.1molMnO2 与含4molHCl的浓盐酸充分反应,能收集到标况下Cl2 小于 22.4L
C.可以用澄清石灰水来吸收含Cl2的尾气
D.84消毒液可以和洁厕剂混合使用
 答案
答案
B、1molMnO2 与含4molHCl的浓盐酸充分反应,能收集到标况下Cl2 小于 22.4L
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“下列说法正确的是()”相关的问题
更多“下列说法正确的是()”相关的问题
A.搅拌后加热前一定是饱和溶液
B.搅拌后加热前一定是不饱和溶液
C.加热后一定是饱和溶液
D.加热后一定是不饱和溶液
A.有机物都是含碳元素的化合物,则含碳元素的化合物一定是有机物
B.保持温度一定,往氢氧化钙饱和溶液中加氧化钙,溶质、溶液的质量一定减少
C.某物质在空气中燃烧生成二氧化碳和水,说明该物质含碳、氢、氧三种元素
D.酸溶液一定显酸性,则显酸性的溶液一定是酸溶液
电解工作原理的实际应用非常广泛。
(1)请画出铜棒镀银的简易装置设计图()。(实验可选用品:铜棒,银片,石墨棒,硫酸铜溶液,硝酸银溶液,导线,电源,烧杯)。
(2)工业上为了处理含有Cr2O12-的酸性工业废水,采用下面的处理方法:往工业废水中加入适量NaCl,以铁为电极进行电解,经过一段时间,有Cr(OH)3和Fe(OH)3沉淀生成,工业废水中铬元素的含量可低于排放标准。关于上述方法,下列说法错误的是()(填字母)。
A、阳极反应:Fe-2e-=Fe2+
B、阴极反应:2H++2e-=H2↑
C、在电解过程中工业废水由酸性变为碱性
D、可以将铁电极改为石墨电极
(3)某同学设计了如图装置进行以下电化学实验。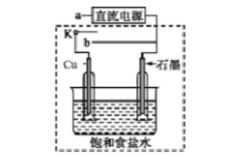 ①当开关K与a连接时,两极均有气泡产生,则阴极为()电极。
①当开关K与a连接时,两极均有气泡产生,则阴极为()电极。
②一段时间后,使开关K与a断开,与b连接时,虚线框内的装置可称为()。请写出此时Cu电极上的电极反应()。
(4)某溶液中含有的离子如下表: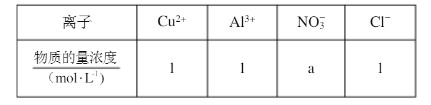 用惰性电极电解该溶液,当电路中有3mole-通过时(忽略电解时溶液体积变化及电极产物可能存在的溶解现象),下列说法正确的是()(填字母)。
用惰性电极电解该溶液,当电路中有3mole-通过时(忽略电解时溶液体积变化及电极产物可能存在的溶解现象),下列说法正确的是()(填字母)。
A、电解后溶液呈酸性
B、a=3
C、阳极生成1.5molCl2
D、阴极析出的金属是铜与铝
A.属于正当防卫,不负刑事责任
B.属于意外事件,不负刑事责任
C.属于防卫过当,应当负刑事责任
D.属于故意杀人,应当负刑事责任
A.质量浓度为4 mg/mL的对氨基苯磺酸溶液呈酸性
B.对氨基苯磺酸溶液和N 1 萘基乙二胺盐酸盐溶液,应避光保存
C.质量浓度为5 μg/mL的亚硝酸钠溶液应保持弱碱性
D.制备样品处理液,加入氢氧化铝的目的是中和氢氧化钠
A.某雨水的pH=5.6,说明该雨水为酸雨
B.某固体中滴加稀盐酸时有气泡产生,说明该固体中一定含有碳酸根离子
C.某溶液能使酚酞试液变红,说明该溶液一定是碱性溶液
D.燃着的木条伸入某无色气体中很快熄灭,说明该气体一定是二氧化碳
A.溶液是均一、稳定、无色、透明的混合物
B.溶液中的溶质可以不止一种
C.75%的酒精溶液中,酒精的比水的多,因此酒精是溶剂
D.将某物质的饱和溶液升高温度就一定能得到该物质的不饱和溶液
A.不饱和溶液转化为饱和溶液,其溶液质量分数一定增大
B.饱和溶液析出晶体后其溶质质量分数一定减少
C.温度升高,某饱和溶液中溶质的质量分数一定减少
D.降温时饱和溶液可能无晶体析出
A.降温时,饱和溶液可能不析出晶体
B.饱和溶液中析出晶体后,浓度一定减小
C.一定温度下,向某饱和溶液中加该溶质,其浓度一定增大
D.不饱和溶液转化为饱和溶液,其浓度一定增大
A.溶质的标准态化学势相同
B.溶质的活度相同
C.溶质的活度系数相同
D.溶质的化学势相同