 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
10mol理想气体由298.15K,1×106Pa自由膨胀到298K,1×105Pa,再经等温可逆压缩到始态,求循环过程的Q,W,△U及△H。
10mol理想气体由298.15K,1×106Pa自由膨胀到298K,1×105Pa,再经等温可逆压缩到始态,求循环过程的Q,W,△U及△H。
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
10mol理想气体由298.15K,1×106Pa自由膨胀到298K,1×105Pa,再经等温可逆压缩到始态,求循环过程的Q,W,△U及△H。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“10mol理想气体由298.15K,1×106Pa自由膨胀到…”相关的问题
更多“10mol理想气体由298.15K,1×106Pa自由膨胀到…”相关的问题
298.15K,1x10-3m3容器中的压力值,并与用理想气体状态方程计算的压力值进行比较.
298.15K时,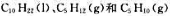 的标准摩尔燃烧焓分别为-6752kJ·mol- 1、-3492kJ·mol-1和-3364kJ·mol-1。计算298.15K裂解反应
的标准摩尔燃烧焓分别为-6752kJ·mol- 1、-3492kJ·mol-1和-3364kJ·mol-1。计算298.15K裂解反应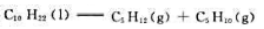 的标准摩尔焓变。
的标准摩尔焓变。
把下列溶液的H2O+浓度换算成pH:
(1)胃液中H3O+浓度为4.0×10-mol·L-1;
(2)人体血液中H3O+浓度为4.0×10mol·L-1;
(3)人的泪液中H3O+浓度为3.2×10mol·L-1。
A.-195kJ·mol-1
B.195kJ·mol-1
C.-875kJ·mol-1
D.875kJ·mol-1
A.△rHөm<0,△rSөm>0
B.△rHөm>0,△rSөm>0
C.△rSөm<0,△rHөm>0
D.△rGөm(298.15K)<0
s)=H3(g)+H2S(g).容器内的总压是66.7kPa,一些固体,NH4HS保留在容器中.计算:(1)298.15K时的K值;(2)固体,NH4HS的分解率;(3)如果容器体积减半,容器中周体,NH4HS物质的量如何变化?
某平动能级间隔为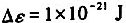 ,假设能级的简并度均为1,则其相邻能级上的粒子数之比在10K时为
,假设能级的简并度均为1,则其相邻能级上的粒子数之比在10K时为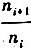 (10K)=();100K时为
(10K)=();100K时为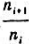 (100K)=(),298.15K时为
(100K)=(),298.15K时为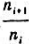 (298.15.K)=().1000K时为
(298.15.K)=().1000K时为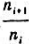 (1000K)=().计算结果的趋势说明().
(1000K)=().计算结果的趋势说明().