 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
已知下列电对的标准电极电势:在酸性溶液中分别用1.0mol·L-1Fe2+,1.0mol·L-1
已知下列电对的标准电极电势:
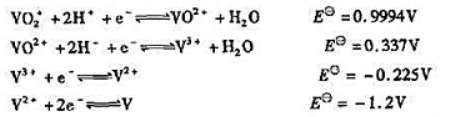
在酸性溶液中分别用1.0mol·L-1Fe2+,1.0mol·L-1Sn2+和Zn还原1.0mol·L-1的VO2+时,最终得到的产物各是什么(不必计算)?
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知下列电对的标准电极电势:
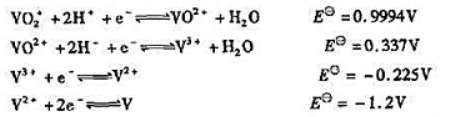
在酸性溶液中分别用1.0mol·L-1Fe2+,1.0mol·L-1Sn2+和Zn还原1.0mol·L-1的VO2+时,最终得到的产物各是什么(不必计算)?
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“已知下列电对的标准电极电势:在酸性溶液中分别用1.0mol·…”相关的问题
更多“已知下列电对的标准电极电势:在酸性溶液中分别用1.0mol·…”相关的问题
查表写出下列电极反应的标准电极电势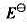 据此回答下列问题:
据此回答下列问题:
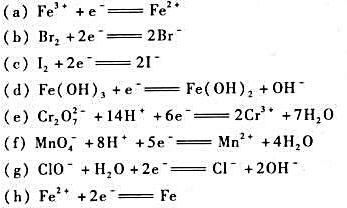
(1)哪些电极反应的电极电势值不受介质的酸碱性影响?
(2)哪种物质是酸性介质中最强的氧化剂?哪种物质是碱性介质中最强的还原剂?
(3)在标准状态下,哪些物质可以将Br-氧化?
(4)在标准状态下,哪些物质可以将Fe3+还原?
(5)降低pH,哪些电极反应的电极电势值升高?
A.Fe3+和Cu
B.Fe2+和Sn2+
C.Cu2+和Fe
D.Fe3+和Fe
A.电极电势是指电极与溶液之间的界面电位差,它可由实验测出
B.还原电极电势越高,该电极氧化态物质得到电子的能力越强
C.电极电势只与电极材料有关,与温度无关
D.电极电势就是标准电极电势
已知下列电极反应的标准电极电势:
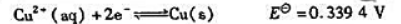
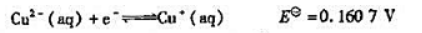
(1)计算反应: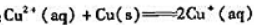 的KΘ;
的KΘ;
(2)已知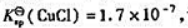 计算反应:
计算反应:
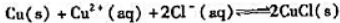 的标准平衡常数KΘ:
的标准平衡常数KΘ:
已知298K时,Ca(OH)2(s)的 =-897.5kJ·mol-1,H2O(1)的
=-897.5kJ·mol-1,H2O(1)的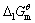 =-237.1kJ·mol-1,
=-237.1kJ·mol-1,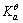 = 1.00×10-7,试求电对Ca(OH)2/Ca的电极电势。
= 1.00×10-7,试求电对Ca(OH)2/Ca的电极电势。
在电对 中,如果H+浓度增大,电极电势增大的是(),电极电势不变的是()。
中,如果H+浓度增大,电极电势增大的是(),电极电势不变的是()。
甲烷燃烧过程可设计成燃料电池.当电解质为酸性溶液时,电极反应和电池反应分别为
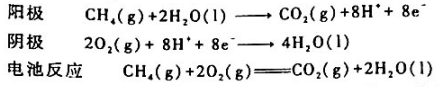
已知,25°C时有关物质的标准摩尔生成吉布斯函数 为
为
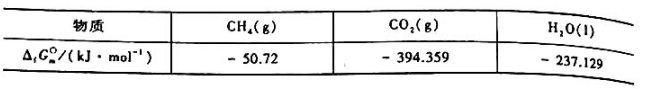
计算25°C时该电池的标准电动势.