 更多“在配位化合物中,中心原子的配位数一定等于配体的数目。()”相关的问题
更多“在配位化合物中,中心原子的配位数一定等于配体的数目。()”相关的问题
第2题
关于分子结构的价键理论,以下正确的是()。
A.中心离子和配位体与配位键结合,其中配体的配原子提供孤对电子是电子的供体,中心离子提供容纳孤对电子的空轨道是电子的受体中心离子必须具有适当的空轨道
B.为增加成键能力,中心原子中能量相近的几个空轨道进行杂化,形成相同数目的,或者是能量相等,并且有一定方向性的杂化轨道
C.配离子的空间结构、配位数以及稳定性主要取决于杂化轨道的数目和类型
D.杂化轨道的数目和类型包括外轨型配合物中心原子使用外层的ns、np和nd轨道进行杂化
第3题
对中心原子的配位数,下列说法不正确的是()。
A.能直接与中心原子配位的原子数目称为配位数
B.中心原子电荷越高,配位数就越大
C.中性配体比阴离子配体的配位数大
D.配位体的半径越大,配位数越大
第5题
试写出八面体结构的配位化合物[CoCl2(NH3)4]Cl的中文名称,并回答下列各问: (1)试
试写出八面体结构的配位化合物[CoCl2(NH3)4]Cl的中文名称,并回答下列各问: (1)试
点击查看答案
试写出八面体结构的配位化合物[CoCl2(NH3)4]Cl的中文名称,并回答下列各问:
(1)试画出配位单元[CoCl2(NH3)4]+的几何异构体;
(2)实验测得此配位化合物的磁矩μ=0μB。试根据配位化合物的价键理论,画出中心钴离子的d电子在轨道中的排布示意图;
(3)写出中心钴离子在成键过程中所用的杂化轨道。
第9题
Fe3+的配位化合物[Fe(CN)6]3-比Fe2+的配位化合物[Fe(CN)6]4-⊕
Fe3+的配位化合物[Fe(CN)6]3-比Fe2+的配位化合物[Fe(CN)6]4-⊕
点击查看答案
Fe3+的配位化合物[Fe(CN)6]3-比Fe2+的配位化合物[Fe(CN)6]4-
稳定,但与邻二氮菲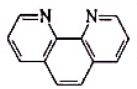 (简写成phen)生成的配位化合物
(简写成phen)生成的配位化合物
[Fe(phen)3]3+不如Fe(phen)3]2+稳定。试解释其原因。
第11题
钯(Pd)与硫代米蚩酮反应生成1:4的有色配位化合物,用1.00cm吸收池在520nm处测得浓度为0.200x10
钯(Pd)与硫代米蚩酮反应生成1:4的有色配位化合物,用1.00cm吸收池在520nm处测得浓度为0.200x10
点击查看答案
-6g/ml的Pd溶液的吸光度值为0.390,试求钯-硫代米蚩酮配合物的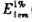 及ε值。(钯-硫代米蚩酮配合物的摩尔质量为106.4)
及ε值。(钯-硫代米蚩酮配合物的摩尔质量为106.4)


 如果结果不匹配,请
如果结果不匹配,请 


















