 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
298K时,反应BaCl2·2H2O(s)BaCl2(s)+2H2O(g)达到平衡时,p(H2O)=330Pa,求
298K时,反应BaCl2·2H2O(s) BaCl2(s)+2H2O(g)达到平衡时,p(H2O)=330Pa,求反应的
BaCl2(s)+2H2O(g)达到平衡时,p(H2O)=330Pa,求反应的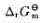 。
。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
298K时,反应BaCl2·2H2O(s) BaCl2(s)+2H2O(g)达到平衡时,p(H2O)=330Pa,求反应的
BaCl2(s)+2H2O(g)达到平衡时,p(H2O)=330Pa,求反应的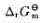 。
。
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“298K时,反应BaCl2·2H2O(s)BaCl2(s)+…”相关的问题
更多“298K时,反应BaCl2·2H2O(s)BaCl2(s)+…”相关的问题
已知下列各反应298K时的自由能改变量:
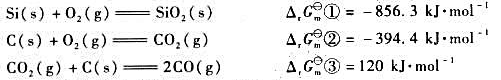
(1)试通过计算说明,制备单质Si的反应:
SiO2(s)+2C(s)=Si(s)+2CO(g)
在常温下不能自发进行。
(2)查热力学数据表,计算上述制备反应的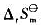 ,进一步计算该反应进行的最低温度要求。
,进一步计算该反应进行的最低温度要求。
已知反应SnO2(s)+2H2(g)=Sn(s)+2H2O(g)和CO(g)+H2O(g)=CO2(g)+H2(g)的平衡常数分别为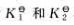 。则反应SnO2(s)+2CO(g)=2CO2(g)+Sn(s)
。则反应SnO2(s)+2CO(g)=2CO2(g)+Sn(s)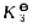 的=()。
的=()。
已知铅酸蓄电池
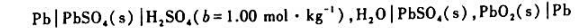
在25°C时的电动势E=1.9283V,Eθ=2.0501V.该电池的电池反应为
Pb(s)+PbO2(s)+2SO42-+4H+→2PbSO4(s)+2H2O
(1)请写出该电池的电极反应;
(2)计算该电池中硫酸溶液的活度a、平均离子活度az及平均离子活度因子γz;
(3) 已知该电池的温度系数为5.664x10-5V·K-1,计算电池反应的ΔrGm,ΔrSm,ΔrHm,
及可逆热Qr,m.
植物在光合作用中合成葡萄糖的反应可以近似表示为:
6CO2(g)+6H2O(1)=C6H12O6(s)+6O2(g)
计算反应的标准摩尔吉布斯自由能,判断反应在298K及标准状态下能否自发进行,已知葡萄糖的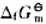 (C6H12O6·s) =-910.5kJ·mol-1。
(C6H12O6·s) =-910.5kJ·mol-1。
半导体工业生产单质硅的过程中有三个重要反应:
(1)二氧化硅被还原为粗硅:SiO2(g)+2C(s)→Si(s)+2CO(g)
(2)硅被氯氧化成四氯化硅:Si(s)+2Cl2(g)→SiCl4(g)
(3)四氯化硅被镁还原生成纯硅:SiCl4(g)+2Mg(s)→2MgCl2(s)+Si(g)
计算上述各反应的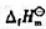 (298K)和生产1.00kg纯硅的总反应热.
(298K)和生产1.00kg纯硅的总反应热.
根据表中给出的298K时的热力学数据:

试求算下面反应:

298K时的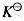 和该温度下固体表面平衡水汽分压。
和该温度下固体表面平衡水汽分压。