 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在真空的容器中放人NH4HS(s),于25℃下分解为NH3(g)与H2S(g),平衡时容器内的压力为6
6.66kPa.
(1)当放入NH4HS(s)时容器内已有39.99kPa的H2S(g),求平衡时容器中的压力;
(2)容器内原有6.666kPa的NH3(g),问H2S压力为多大时才能形成NH4HS(s)?
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
6.66kPa.
(1)当放入NH4HS(s)时容器内已有39.99kPa的H2S(g),求平衡时容器中的压力;
(2)容器内原有6.666kPa的NH3(g),问H2S压力为多大时才能形成NH4HS(s)?
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“在真空的容器中放人NH4HS(s),于25℃下分解为NH3(…”相关的问题
更多“在真空的容器中放人NH4HS(s),于25℃下分解为NH3(…”相关的问题
s)=H3(g)+H2S(g).容器内的总压是66.7kPa,一些固体,NH4HS保留在容器中.计算:(1)298.15K时的K值;(2)固体,NH4HS的分解率;(3)如果容器体积减半,容器中周体,NH4HS物质的量如何变化?
指出下列平衡系统中的组分数C,相数P及自由度F.
(1)l2(s)与其蒸气成平衡:
(2)MgCO3(s)与其分解产物MgO(s)和CO2(g)成平衡;
(3)NH4CI(s)放入一抽空的容器中,与其分解产物NH3(g)和HCI(g)成平衡;
(4)任意量的NH3(g)和H2S(g)与NH4HS(s)成平衡;
(5)过量的NH4HCO3(s)与其分解产物NH3(g),H2O(g)和CO2(g)成平衡;
(6)I2作为溶质在两不互溶液体H2O和CCI4中达到分配平衡(凝聚系统).
,此时系统的平衡压力为104.67kPa.在同样的条件下,若放人的是NH4I(s),则测得的平衡压力为18.864kPa,试求当NH4CI(s)和NH4I(s)同时存在时,反应系统在340℃下达平衡时的总压.设HI(g)不分解,且此两种盐类不形成固溶体.
在100℃下,于装有NH3(g)的密封容器中放入过量的NH4Cl(s),NH4Cl(s)发生分解反应:
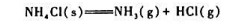
则系统的组分数C=(),相数P=(),自由度F=().
A.CO(g)+Cl2(g)→COCl2(g)
B.2NO2(g)→NO(g)+1/2O2(g)
C.N2(g)+O2(g)→2NO(g)
D.NH4HS(s)→NH3(g)+H2S(g)
已知水在100℃,101.325kPa下的摩尔蒸发焓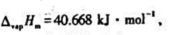 试分别计算下列两过程的Q,W,ΔU和△H.(水蒸气可按理想气体处理.)
试分别计算下列两过程的Q,W,ΔU和△H.(水蒸气可按理想气体处理.)
(1)在100℃,101.325kPa条件下,1kg水蒸发为水蒸气;
(2)在恒定100℃的真空容器中,1kg水全部蒸发为水蒸气,并且水蒸气压力恰好为101.325kPa.
A.煮沸10min可杀灭多数细菌芽胞
B.物品需全部浸入水中f相同的容器应重叠放在一起
C.橡胶类物品在冷水中或温水中放人
D.中途加入其他物品,需等再次水沸后计时
E.在水中加入亚硝酸钠可提高杀菌效果