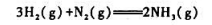题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
[主观题]
298.15K,101.325kPa下,1mol过饱和水蒸气变为同温同压下的液态水.求此过程的ΔS及ΔG,并判断此过程能否自动进行.已知298.15K时水的饱和蒸气压为3.166kPa,质量蒸发焓为2217J·g-1.
查看答案
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
 如果结果不匹配,请 联系老师 获取答案
如果结果不匹配,请 联系老师 获取答案
 更多“298.15K,101.325kPa下,1mol过饱和水蒸气…”相关的问题
更多“298.15K,101.325kPa下,1mol过饱和水蒸气…”相关的问题
已知298.15K时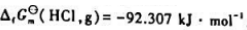 化学反应
化学反应
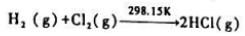
在催化剂的作用下反应速率大大加快时,反应的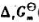 (298.15K)=().
(298.15K)=().
A.△rHөm<0,△rSөm>0
B.△rHөm>0,△rSөm>0
C.△rSөm<0,△rHөm>0
D.△rGөm(298.15K)<0
已知水在101.325kPa,100℃下的摩尔蒸发焓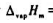 =40.668kJ·mol-1,现有2mol水蒸气在100℃,101.325kPa条件下凝结为液体水,此过程的ΔH=()kJ,Q=()kJ,W=()kJ,ΔU=()kJ.
=40.668kJ·mol-1,现有2mol水蒸气在100℃,101.325kPa条件下凝结为液体水,此过程的ΔH=()kJ,Q=()kJ,W=()kJ,ΔU=()kJ.
298.15K时,水蒸气的标准摩尔生成吉布斯函数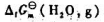 =-228.572kJ·mol-1.在同样温度下,反应
=-228.572kJ·mol-1.在同样温度下,反应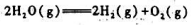 的标准平衡常数Kθ=().
的标准平衡常数Kθ=().
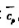 .已知水在100℃,101.325kPa下的摩尔蒸发焓
.已知水在100℃,101.325kPa下的摩尔蒸发焓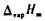 =40.668kJ·mol-1,水的平均摩尔定压热容
=40.668kJ·mol-1,水的平均摩尔定压热容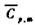 =75·32J·mol-1·K-1.
=75·32J·mol-1·K-1.
已知水在100℃,101.325kPa下的摩尔蒸发焓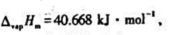 试分别计算下列两过程的Q,W,ΔU和△H.(水蒸气可按理想气体处理.)
试分别计算下列两过程的Q,W,ΔU和△H.(水蒸气可按理想气体处理.)
(1)在100℃,101.325kPa条件下,1kg水蒸发为水蒸气;
(2)在恒定100℃的真空容器中,1kg水全部蒸发为水蒸气,并且水蒸气压力恰好为101.325kPa.
A.在温度升高至一定数值以上即可自发进行
B.在温度降低至一定数值以上即可自发进行
C.在任何温度下反应都能自发进行
D.在任何温度下反应都不能自发进行